बैटरी और वे कैसे काम करते हैं। परिचालन सिद्धांत
समय के साथ, वे अपना शुल्क खर्च करते हैं, और इसे समय-समय पर बहाल किया जाना चाहिए। इस प्रक्रिया के पहलुओं पर लेख में चर्चा की जाएगी।
चार्जिंग किसे कहते हैं
यह प्रक्रिया का नाम है, जो निर्वहन के विपरीत है। चार्जिंग के दौरान, सीलबंद लीड-एसिड बैटरी को ऊर्जा के साथ संग्रहित किया जाता है, जबकि बाहरी करंट स्रोत द्वारा संचालित किया जाता है। अंतिम परिणाम चार्ज का संचय है, जो समाई के बराबर है। वो कैसे दिखते हैं चार्जिंग डिवाइससीलबंद लीड एसिड बैटरी के लिए? वे एक ऊर्जा कनवर्टर और दो आउटपुट हैं, जिनमें से प्रत्येक एक सीलबंद, रखरखाव-मुक्त लीड-एसिड बैटरी से जुड़ा है, जब नेटवर्क से जुड़ा होता है, तो यह पुनर्प्राप्ति और परिवर्तन की प्रक्रिया शुरू कर देगा विद्युतीय ऊर्जा(नेटवर्क से आपूर्ति) रसायन के लिए। ताकि भविष्य में जरूरत पड़ने पर वह उलटी प्रक्रिया को अंजाम दे सके और विभिन्न उपकरणों और उपकरणों को शक्ति प्रदान कर सके।
आसानी से और सुरक्षित रूप से चार्ज करना
 ऐसा करने के लिए, आपको "वर्तमान-वोल्टेज" विधि का उपयोग करने की आवश्यकता है। यह क्या है? प्रारंभ में, बैटरी को डायरेक्ट करंट से चार्ज किया जाता है। जब आवश्यक संकेतक प्राप्त हो जाते हैं, तो समर्थन जाना शुरू हो जाता है स्थिर वोल्टेज. प्रारंभिक चार्जिंग करंट का पता लगाने के लिए, आमतौर पर मामले की सावधानीपूर्वक जांच करने के लिए पर्याप्त है - यह पैरामीटर वहां इंगित किया गया है। आमतौर पर यह मान 0.3 तक होता है इसे और स्पष्ट करने के लिए, आइए कल्पना करें कि हमारे पास 100 ए / एच के पैरामीटर वाला एक उपकरण है। तब चार्ज करंट 30A से अधिक नहीं होना चाहिए। लेकिन यह एक सुरक्षित अधिकतम है, कई निर्माता अपने चार्जर में दस प्रतिशत नियम का उपयोग करते हैं। यह आपको कुछ गलत करने और इसे नुकसान पहुंचाने के कम से कम डर के बिना बैटरी चार्ज करने की अनुमति देता है। आपको कितना चार्ज करने की आवश्यकता है? यदि प्रारंभिक धारा 20% क्षमता है, तो बैटरी आरक्षित लगभग 5-6 घंटों में 90% तक बहाल हो जाएगी। शेष 10% में लगभग एक दिन लगेगा। इसकी कार्यप्रणाली की ये विशेषताएं हैं कि सीलबंद लीड-एसिड बैटरी के चार्जर में है। क्या इस प्रक्रिया को तेज करने का कोई तरीका है? हाँ, और अब हम देखेंगे कि कैसे।
ऐसा करने के लिए, आपको "वर्तमान-वोल्टेज" विधि का उपयोग करने की आवश्यकता है। यह क्या है? प्रारंभ में, बैटरी को डायरेक्ट करंट से चार्ज किया जाता है। जब आवश्यक संकेतक प्राप्त हो जाते हैं, तो समर्थन जाना शुरू हो जाता है स्थिर वोल्टेज. प्रारंभिक चार्जिंग करंट का पता लगाने के लिए, आमतौर पर मामले की सावधानीपूर्वक जांच करने के लिए पर्याप्त है - यह पैरामीटर वहां इंगित किया गया है। आमतौर पर यह मान 0.3 तक होता है इसे और स्पष्ट करने के लिए, आइए कल्पना करें कि हमारे पास 100 ए / एच के पैरामीटर वाला एक उपकरण है। तब चार्ज करंट 30A से अधिक नहीं होना चाहिए। लेकिन यह एक सुरक्षित अधिकतम है, कई निर्माता अपने चार्जर में दस प्रतिशत नियम का उपयोग करते हैं। यह आपको कुछ गलत करने और इसे नुकसान पहुंचाने के कम से कम डर के बिना बैटरी चार्ज करने की अनुमति देता है। आपको कितना चार्ज करने की आवश्यकता है? यदि प्रारंभिक धारा 20% क्षमता है, तो बैटरी आरक्षित लगभग 5-6 घंटों में 90% तक बहाल हो जाएगी। शेष 10% में लगभग एक दिन लगेगा। इसकी कार्यप्रणाली की ये विशेषताएं हैं कि सीलबंद लीड-एसिड बैटरी के चार्जर में है। क्या इस प्रक्रिया को तेज करने का कोई तरीका है? हाँ, और अब हम देखेंगे कि कैसे।
सीलबंद लीड-एसिड बैटरी की तेजी से चार्जिंग
मान 13.8 के वोल्टेज पर प्रत्यक्ष धारा के साथ चार्ज हो रहा है। संभावित नकारात्मक प्रभावों के कारण अब इसकी अनुशंसा नहीं की जाती है। लेकिन अगर वे आपको डराते नहीं हैं, तो आप वोल्टेज को 14.5 V तक बढ़ा सकते हैं (यह 12 V बैटरी के लिए है)। नतीजतन, बैटरी 20% की दर से 6 घंटे में चार्ज हो जाएगी। चक्रीय मोड में काम करते समय इस पद्धति का विशेष रूप से उपयोग किया जाता है।
तापमान प्रभाव
 ऊपर जो कुछ भी लिखा गया था वह केवल उस स्थिति पर लागू होता है जब तापमान 20 डिग्री सेल्सियस होता है। अन्य संकेतकों के लिए, मुआवजे की शुरुआत करना आवश्यक है चार्जिंग वोल्टेज. लेड-एसिड बैटरी को -15 से 40 डिग्री तक चार्ज किया जा सकता है। तापमान जितना अधिक होगा, ओवरचार्जिंग से बचने के लिए वोल्टेज उतना ही कम होना चाहिए। अन्यथा, यह आंकड़ा, इसके विपरीत, अंडरचार्जिंग से बचने के लिए बढ़ाया जाना चाहिए। इस वजह से, एक सीलबंद, रखरखाव-मुक्त लीड-एसिड बैटरी को ठीक 20 डिग्री सेल्सियस, प्लस या माइनस कुछ की स्थितियों में चार्ज करने की सलाह दी जाती है। बेशक, आप हर बार गणना कर सकते हैं, लेकिन यह हमेशा सुविधाजनक नहीं होता है। उनके घरों को अक्सर तापमान पैरामीटर के लिए आदर्श स्थान के रूप में चुना जाता है, लेकिन फिर इस प्रक्रिया के दौरान और इसके समाप्त होने के कुछ घंटों बाद चार्जिंग स्थान के उच्च-गुणवत्ता वाले वेंटिलेशन का ध्यान रखना आवश्यक है।
ऊपर जो कुछ भी लिखा गया था वह केवल उस स्थिति पर लागू होता है जब तापमान 20 डिग्री सेल्सियस होता है। अन्य संकेतकों के लिए, मुआवजे की शुरुआत करना आवश्यक है चार्जिंग वोल्टेज. लेड-एसिड बैटरी को -15 से 40 डिग्री तक चार्ज किया जा सकता है। तापमान जितना अधिक होगा, ओवरचार्जिंग से बचने के लिए वोल्टेज उतना ही कम होना चाहिए। अन्यथा, यह आंकड़ा, इसके विपरीत, अंडरचार्जिंग से बचने के लिए बढ़ाया जाना चाहिए। इस वजह से, एक सीलबंद, रखरखाव-मुक्त लीड-एसिड बैटरी को ठीक 20 डिग्री सेल्सियस, प्लस या माइनस कुछ की स्थितियों में चार्ज करने की सलाह दी जाती है। बेशक, आप हर बार गणना कर सकते हैं, लेकिन यह हमेशा सुविधाजनक नहीं होता है। उनके घरों को अक्सर तापमान पैरामीटर के लिए आदर्श स्थान के रूप में चुना जाता है, लेकिन फिर इस प्रक्रिया के दौरान और इसके समाप्त होने के कुछ घंटों बाद चार्जिंग स्थान के उच्च-गुणवत्ता वाले वेंटिलेशन का ध्यान रखना आवश्यक है।
सुरक्षा सावधानियों का पालन न करने के परिणाम
ऊपर वर्णित विधियों का उद्देश्य तेज और सुरक्षित चार्जिंग है। साथ ही, कार्य एक लीड-एसिड बैटरी के जीवनकाल को उसके उम्र बढ़ने के कारकों को कम करके अधिकतम करना है। अब आइए विचलन को देखें। यदि आप अधिकतम अनुमेय से अधिक करंट का उपयोग करते हैं तो क्या होता है? प्रारंभ में, यह ध्यान दिया जाना चाहिए कि सीलबंद लीड-एसिड बैटरी पूरी तरह चार्ज करने में सक्षम नहीं होंगी। इसके अलावा, गैस पुनर्संयोजन तंत्र की दक्षता में कमी के कारण, इलेक्ट्रोलाइट पानी खो देगा। इसलिए, एक भी चार्ज काम के संसाधन को कम करने के लिए पर्याप्त है।
लेकिन क्या होगा अगर आप करंट को क्षमता के 0.5 प्रतिशत तक कम कर दें? इस मामले में भी सीलबंद लीड-एसिड बैटरी चार्ज होगी, लेकिन यह प्रक्रिया कई हफ्तों तक जारी रहेगी। इसके अलावा, डिवाइस एक ऐसी स्थिति में होगा जो डिस्चार्ज होने के बराबर है। और यह सल्फेशन की ओर जाता है और त्वरित उम्र बढ़ने. बेशक, एक छोटे से करंट के साथ एक चार्ज गंभीर क्षति के लिए पर्याप्त नहीं है, लेकिन बेहतर है कि उनका उपयोग न करें। अंतिम वोल्टेज की निगरानी करना भी आवश्यक है ताकि डिवाइस का कम चार्ज न हो और इसके संसाधन में कमी न हो।
और चार्ज करने के लिए लीड-एसिड बैटरी में इतनी तापमान सीमा क्यों होती है? तथ्य यह है कि उन्हें छोड़ते समय, गैस पुनर्संयोजन तंत्र का संचालन बंद हो जाता है, और इलेक्ट्रोलाइट अपना पानी खो देता है।
क्या सब कुछ ठीक था

प्राप्त होना अच्छा परिणाम, आवश्यक सीमा के भीतर आवश्यक मापदंडों का पालन करना आवश्यक है। इस मामले में मुख्य स्थान पर वर्तमान और वोल्टेज का कब्जा होना चाहिए (तापमान पर विचार करें)। फिर सीलबंद लीड-एसिड बैटरी सफलतापूर्वक चार्ज हो जाएंगी और लंबे समय तक चलने में सक्षम होंगी। यदि आसपास इलेक्ट्रोलाइट है, सफेद जमा या बुलबुले हैं, तो डिवाइस की विशेषताओं की बहाली गलत तरीके से की गई थी। आप स्थिति निर्धारित करने के लिए एक परीक्षक का उपयोग कर सकते हैं। सीलबंद लीड-एसिड बैटरी की बहाली विशेष चार्जर (जिसमें कई दिन लग सकते हैं) या अतिरिक्त यांत्रिक क्रियाओं (किसी तरह इलेक्ट्रोलाइट जोड़ें) का उपयोग करके किया जाता है।
निष्कर्ष
 जैसा कि आप देख सकते हैं, लीड-एसिड बैटरी चार्ज करने की प्रक्रिया मुश्किल नहीं है। यदि सुरक्षा सावधानियों का पालन किया जाता है, तो कुछ गलत करना आसान नहीं होगा। लेकिन अंत में, मैं उन्हें अलग-अलग कमरों में चार्ज करने की सलाह देना चाहूंगा, और यदि उपकरणों को आवासीय भवन में बहाल किया जाता है, तो आपको प्रक्रिया के दौरान उच्च गुणवत्ता वाले वेंटिलेशन का ध्यान रखना होगा, साथ ही इसके कई घंटे बाद भी। ये सुरक्षा उपाय इस तथ्य के कारण आवश्यक हैं कि, सूक्ष्म खुराक में, सीसा हवा में प्रवेश कर सकता है, और इसके माध्यम से शरीर में, जहां से यह बहुत धीरे-धीरे उत्सर्जित होता है और लगातार विषाक्त प्रभाव डालता है।
जैसा कि आप देख सकते हैं, लीड-एसिड बैटरी चार्ज करने की प्रक्रिया मुश्किल नहीं है। यदि सुरक्षा सावधानियों का पालन किया जाता है, तो कुछ गलत करना आसान नहीं होगा। लेकिन अंत में, मैं उन्हें अलग-अलग कमरों में चार्ज करने की सलाह देना चाहूंगा, और यदि उपकरणों को आवासीय भवन में बहाल किया जाता है, तो आपको प्रक्रिया के दौरान उच्च गुणवत्ता वाले वेंटिलेशन का ध्यान रखना होगा, साथ ही इसके कई घंटे बाद भी। ये सुरक्षा उपाय इस तथ्य के कारण आवश्यक हैं कि, सूक्ष्म खुराक में, सीसा हवा में प्रवेश कर सकता है, और इसके माध्यम से शरीर में, जहां से यह बहुत धीरे-धीरे उत्सर्जित होता है और लगातार विषाक्त प्रभाव डालता है।
प्रतिश्रेणी:
वाहन विद्युत उपकरण
शीशा अम्लीय बैटरी
लीड-एसिड बैटरी के संचालन का सिद्धांत
बैटरी कहा जाता है विद्युत उपकरण, जो, जब स्रोतों से चार्ज किया जाता है एकदिश धाराविद्युत ऊर्जा जमा करता है, और जब इसे निर्वहन करता है तो यह उपभोक्ताओं को देता है, इस मामले में वर्तमान का स्रोत होता है।
लीड-एसिड बैटरी मुख्य रूप से ऑटोमोबाइल में उपयोग की जाती हैं। उनके अलावा, क्षारीय लौह-निकल बैटरी का भी उपयोग किया जा सकता है।
सबसे सरल लेड-एसिड बैटरी (सेल) एक कांच या प्लास्टिक का जार होता है, जिसमें दो लेड प्लेट नीचे होती हैं और रासायनिक रूप से शुद्ध मजबूत सल्फ्यूरिक एसिड और आसुत जल के इलेक्ट्रोलाइट घोल से भरा होता है। सल्फ्यूरिक एसिड, सीसा प्लेटों पर कार्य करता है, उन्हें ऑक्सीकरण करता है, और प्लेटों की सतह को लेड सल्फेट के लेप से ढक दिया जाता है। इस मामले में, समाधान का घनत्व कम हो जाता है, और इलेक्ट्रोलाइट में लगभग शुद्ध पानी रहता है।
बैटरी को करंट की आपूर्ति करने में सक्षम होने के लिए, इसे पहले चार्ज किया जाना चाहिए, अर्थात, इसके माध्यम से एक निरंतर करंट प्रवाहित किया जाना चाहिए। बिजली. इलेक्ट्रोलाइट के माध्यम से सकारात्मक से नकारात्मक प्लेट में विद्युत प्रवाह के पारित होने के कारण, बैटरी में एक रासायनिक प्रतिक्रिया होती है। इस मामले में, सकारात्मक प्लेट पर लेड सल्फेट को लेड पेरोक्साइड में बदल दिया जाता है, और नकारात्मक प्लेट पर - शुद्ध स्पंजी लेड में, इलेक्ट्रोलाइट में फिर से प्रकट होता है गंधक का तेजाबऔर विलयन का घनत्व बढ़ जाता है।
जब प्लेटों की संरचना का रासायनिक परिवर्तन पूरा हो जाता है, तो बैटरी चार्ज हो जाएगी। यदि आप बैटरी के माध्यम से विद्युत प्रवाह जारी रखते हैं, तो इलेक्ट्रोलाइट पानी अपने घटक भागों - हाइड्रोजन और ऑक्सीजन में विघटित होना शुरू हो जाएगा, जो इलेक्ट्रोलाइट से बुलबुले के रूप में निकलेगा। बुलबुले का तेजी से निकलना (इलेक्ट्रोलाइट उबलना) बैटरी चार्जिंग के अंत का संकेत देता है।
जब किसी आवेशित बैटरी के ध्रुवों को बाहरी परिपथ द्वारा बंद कर दिया जाता है, तो उसमें एक विपरीत रासायनिक प्रतिक्रिया होगी, जिसमें उनकी संरचना में प्लेटें अपनी मूल स्थिति में वापस आ जाएंगी। नतीजतन, बैटरी को डिस्चार्ज कर दिया जाएगा और उपभोक्ताओं को स्विच ऑन करने के लिए संग्रहीत विद्युत ऊर्जा को बंद कर दिया जाएगा। डिस्चार्ज करते समय, बाहरी सर्किट में विद्युत प्रवाह धनात्मक प्लेट से ऋणात्मक की ओर प्रवाहित होगा, अर्थात चार्जिंग के दौरान दिशा के विपरीत दिशा में। इस मामले में, बैटरी की सकारात्मक और नकारात्मक प्लेटों को फिर से लेड सल्फेट की कोटिंग के साथ कवर किया जाएगा, और इलेक्ट्रोलाइट का घनत्व कम हो जाएगा, और यह लगभग बदल जाएगा स्वच्छ जल. जब रासायनिक प्रतिक्रिया पूरी तरह से समाप्त हो जाती है, तो बैटरी डिस्चार्ज हो जाएगी और अधिक विद्युत प्रवाह नहीं दे पाएगी। आगे के संचालन के लिए बैटरी को रिचार्ज करना होगा।
बैटरी डिवाइस
बैटरी से इकट्ठी की जाती है व्यक्तिगत तत्व- सामान्य टैंक-मोनोब्लॉक में संचायक।
कार बैटरी के मोनोब्लॉक को अलग-अलग बैटरी कक्षों में विभाजन द्वारा विभाजित किया जाता है। प्रत्येक कक्ष एक कॉर्क के साथ लिपटे एक भरने वाले छेद के साथ एक इबोनाइट ढक्कन के साथ शीर्ष पर बंद है। कक्ष में विभाजकों द्वारा अलग किए गए प्लेटों (सकारात्मक और नकारात्मक) का एक सेट स्थापित किया गया है।
मोनोब्लॉक डामर-पिच द्रव्यमान या एबोनाइट से बना है। प्लास्टिक (पॉलीविनाइल क्लोराइड या विनाइल प्लास्टिक) से बने पतली दीवार वाले एसिड-प्रतिरोधी आवेषण को आमतौर पर एक डामर-पिच मोनोब्लॉक के कक्षों में दबाया जाता है, जो मोनोब्लॉक की दीवारों को एसिड हमले से अच्छी तरह से बचाता है, जो इसकी सेवा जीवन को काफी बढ़ाता है।
बैटरी की क्षमता बढ़ाने के लिए, यानी चार्ज करते समय अधिक विद्युत ऊर्जा को अवशोषित करने की इसकी क्षमता, प्रत्येक कक्ष में एक विशेष डिजाइन की कई सकारात्मक और नकारात्मक प्लेटें स्थापित की जाती हैं, जिसके परिणामस्वरूप प्लेटों की कुल कार्य सतह बढ़ जाती है।

चावल। 1. लीड-एसिड बैटरी के संचालन की योजना
प्रत्येक प्लेट का आधार यांत्रिक शक्ति को बढ़ाने के लिए सुरमा के एक छोटे से मिश्रण (6-8%) के साथ शुद्ध सीसे से डाली गई जाली है। सक्रिय द्रव्यमान को ग्रेट में दबाया जाता है, फिर इसे सुखाया जाता है। यह द्रव्यमान पाउडर लेड ऑक्साइड से तैयार किया जाता है - लाल लेड और लेड लिथरेज, मजबूत, रासायनिक रूप से शुद्ध सल्फ्यूरिक एसिड के साथ मिश्रित। सकारात्मक प्लेटों के सक्रिय द्रव्यमान में आमतौर पर 75% तक लाल सीसा होता है, और इसलिए प्लेटों में लाल रंग का रंग होता है। नकारात्मक प्लेटों के सक्रिय द्रव्यमान में अधिक लेड लिटर्ज होता है, प्लेटें ग्रे या नीले रंग की होती हैं।
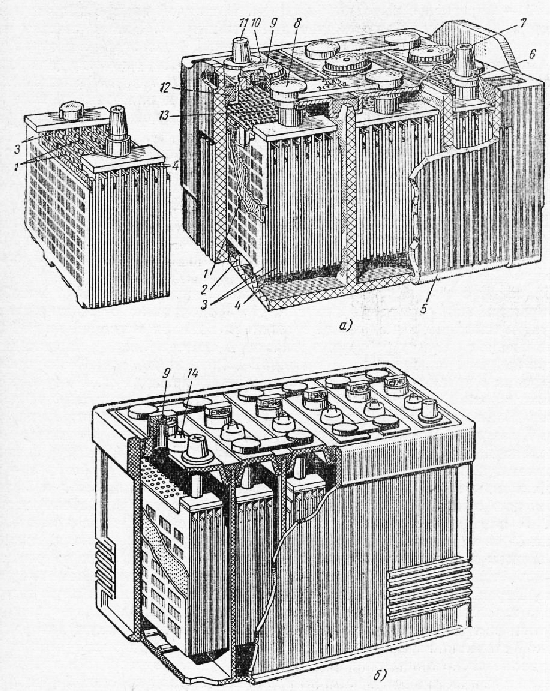
चावल। 2. लीड-एसिड स्टोरेज बैटरी: ए - तीन-तत्व; बी - छह-तत्व
इन लेड ऑक्साइड के अलावा, पाउडर लेड का उपयोग प्लेटों के लिए पैकिंग के रूप में भी किया जाता है, जो पीसने के दौरान ऑक्सीकृत हो जाता है, सल्फ्यूरिक एसिड के साथ उभारा जाता है।
निर्माण और संयोजन के बाद, प्लेटों को मोल्डिंग के अधीन किया जाता है, अर्थात, विद्युत प्रवाह और निर्वहन के साथ चार्ज करने की दोहराई जाने वाली प्रक्रियाएं।
एक ही नाम की सभी प्लेटों को एक सामान्य जम्पर के साथ एक ब्लॉक में वेल्डिंग द्वारा जोड़ा जाता है - एक आउटपुट पिन के साथ एक बैरेट। प्रत्येक कक्ष में, सकारात्मक प्लेटें नकारात्मक के बगल में स्थित होती हैं। प्लेट ब्लॉक में दो आउटपुट पिन (बोरॉन) होते हैं - सकारात्मक (सकारात्मक) और नकारात्मक (नकारात्मक)। प्रत्येक ब्लॉक में सकारात्मक प्लेटों की तुलना में एक नकारात्मक प्लेट होती है। इसलिए, प्रत्येक सकारात्मक प्लेट को दोनों तरफ नकारात्मक प्लेटों द्वारा बंद कर दिया जाता है, जिसके परिणामस्वरूप इसकी पूरी सतह का उपयोग किया जाता है और एक बड़े डिस्चार्ज करंट पर इसके विकृत होने की संभावना समाप्त हो जाती है।
एक प्लेट के दूसरे के साथ सीधे संपर्क को खत्म करने के लिए या उन्हें गिरने वाले सक्रिय द्रव्यमान के साथ बंद करने के लिए, एसिड प्रतिरोधी गास्केट - विभाजक उनके बीच स्थापित होते हैं। दो प्रकार के विभाजक हैं:
1) लकड़ी या संयुक्त मिश्रित से - लकड़ी और विनाइल क्लोराइड से, या लकड़ी और फाइबरग्लास से;
2) माइक्रोपोरस एबोनाइट (मिपोर) और माइक्रोपोरस प्लास्टिक (मिप्लास्ट) से या माइप्लास्ट और विनाइल क्लोराइड से संयुक्त, या माइप्लास्ट और ग्लास-महसूस।
विभाजक के साथ प्लेट्स को मोनोब्लॉक के अलग-अलग कक्षों में स्थापित किया जाता है और तल पर नीचे की पसलियों पर आराम किया जाता है, जो प्लेट के निचले हिस्सों को समय के साथ बाहर गिरने वाले सक्रिय द्रव्यमान द्वारा बंद होने और कीचड़ कक्ष में पसलियों के बीच जमा होने से रोकता है। . ऊपर से प्रत्येक कक्ष को प्लास्टिक के आवरण से कसकर बंद कर दिया जाता है। कवर के साथ जंक्शनों पर मोनोब्लॉक कक्षों के किनारों को एसिड प्रतिरोधी मैस्टिक से भर दिया जाता है। प्रत्येक कक्ष के आवरण की सतह पर प्लेटों के ब्लॉक (बोरॉन) के ऋणात्मक और धनात्मक पिन निकलते हैं। पिन को कवर में एम्बेडेड रिब्ड लीड बुशिंग के साथ सील कर दिया जाता है। झाड़ियों को इंटर-एलिमेंट जंपर्स के साथ पिन में मिलाया जाता है। कुछ प्रकार की बैटरियों में, कैप वाले पिन को एसिड-प्रतिरोधी द्रव्यमान से सील कर दिया जाता है। बैटरी में अंतिम दो पिन - प्लस और माइनस - पोल के टुकड़ों से सुसज्जित हैं, जिससे बाहरी नेटवर्क केबल क्लैम्प और टाई बोल्ट का उपयोग करके जुड़े हुए हैं। प्लेटों के ऊपर प्रत्येक कक्ष में विनाइल क्लोराइड या अन्य एसिड-प्रतिरोधी सामग्री से बने सुरक्षात्मक ढाल होते हैं, जो विभाजकों और प्लेटों के किनारों को यांत्रिक क्षति से बचाने का काम करते हैं। प्रत्येक कक्ष के ढक्कन में एक फिलिंग होल होता है, जो एक सीलिंग गैस्केट पर बंद होता है जिसमें एक प्लग 9 होता है जिसमें एक वेंट होल होता है जो गैसों को छोड़ने का काम करता है। छेद के नीचे प्लग में एक परावर्तक प्लेट लगाई जाती है, जो इलेक्ट्रोलाइट स्प्लैशिंग को समाप्त करती है। नई बैटरियों में, कॉर्क के नीचे एक सीलिंग डिस्क लगाई जाती है, जिसे बैटरी संचालन के दौरान हटा दिया जाता है। कुछ प्रकार की बैटरियों में, इलेक्ट्रोलाइट को भरने के लिए ढक्कन में खोलना गैस्केट पर एक सीलिंग रबर आस्तीन के साथ एक अंधा प्लग के साथ बंद होता है, और गैसों को छोड़ने के लिए एक परावर्तक के साथ एक विशेष वेंटिलेशन फिटिंग होती है। भरने वाले छेद के लिए ऐसा उपकरण इलेक्ट्रोलाइट को आवश्यक स्तर पर जोड़ने के लिए और अधिक सुविधाजनक बनाता है।
बैटरियों को मोल्डेड प्लेटों के साथ उत्पादित किया जाता है, लेकिन आमतौर पर इलेक्ट्रोलाइट के बिना सूखे रूप में। इसलिए, नई बैटरियों को इलेक्ट्रोलाइट से भरा और चार्ज किया जाना चाहिए।
रिचार्जेबल बैटरी एक ब्लॉक में तीन या छह कोशिकाओं के साथ उपलब्ध हैं; बाद के मामले में, वे तत्वों की अनुप्रस्थ या अनुदैर्ध्य व्यवस्था के साथ उत्पन्न होते हैं। ट्रकों के लिए अभिप्रेत बैटरियों को आमतौर पर ढक्कन के साथ लकड़ी के मामले में स्थापित किया जाता है। ऑफ-रोड वाहनों में उपयोग की जाने वाली बैटरियां सीलबंद (हाइड्रोस्टैटिक) प्लग से सुसज्जित होती हैं, जो वाहन के फोर्ड से आगे निकलने पर बैटरी में पानी के प्रवेश की संभावना को समाप्त कर देती हैं।
बैटरी के मुख्य संकेतक
बैटरी और बैटरी के संचालन को निर्धारित करने वाले मुख्य संकेतक इसकी वोल्टेज और क्षमता हैं।
बैटरी की एक बैटरी (तत्व), इसमें प्लेटों की संख्या और उनके आकार की परवाह किए बिना, अच्छी और चार्ज स्थिति में 2 वी का औसत वोल्टेज देती है। पर पूर्ण निर्वहनइसमें वोल्टेज घटकर 1.7 V हो जाता है।
बैटरी की क्षमता चार्जिंग के दौरान अवशोषित करने की इसकी क्षमता है, और फिर अधिकतम स्वीकार्य वोल्टेज ड्रॉप के लिए निरंतर वर्तमान के साथ निर्वहन करते समय एक या दूसरी मात्रा में विद्युत ऊर्जा छोड़ दें।
क्षमता बैंक (कक्ष) में प्लेटों की संख्या और उनके आकार पर निर्भर करती है और इसे एम्पीयर-घंटे (आह) में मापा जाता है। क्षमता का निर्धारण एम्पीयर में डिस्चार्ज करंट को घंटों में उस समय से गुणा करके किया जाता है जब बैटरी को उस करंट पर डिस्चार्ज किया जा सकता है। उदाहरण के लिए, यदि कुछ शर्तों के तहत बैटरी डिस्चार्ज के दौरान 5 घंटे के लिए 4 ए का करंट दे सकती है, तो इसकी क्षमता 20 आह है।
एक बैटरी का वोल्टेज कार के विद्युत उपकरणों को बिजली देने के लिए पर्याप्त नहीं है। एक उच्च वोल्टेज प्राप्त करने के लिए, कई बैटरियों को एक मोनोब्लॉक में एक बैटरी में जोड़ा जाता है और लीड जंपर्स का उपयोग करके श्रृंखला में एक को दूसरे से जोड़ा जाता है। इस मामले में, एक तत्व का सकारात्मक टर्मिनल दूसरे तत्व के नकारात्मक टर्मिनल से जुड़ा होता है, आदि।
जब बैटरियों को श्रृंखला में जोड़ा जाता है, तो बैटरी के चरम आउटपुट टर्मिनलों पर वोल्टेज बैटरियों की संख्या के अनुपात में बढ़ जाता है, और पूरी बैटरी की क्षमता एक बैटरी की क्षमता के बराबर रहती है।
बैटरी के ब्रांड में इंगित क्षमता को नाममात्र क्षमता कहा जाता है और इसे काफी विशिष्ट निर्वहन स्थितियों के तहत प्रदान किया जाता है: 10-घंटे के मोड पर और औसत इलेक्ट्रोलाइट तापमान 30 ° (GOST 959-51)।
बैटरी की क्षमता स्थिर नहीं है। डिस्चार्ज करंट में वृद्धि और इलेक्ट्रोलाइट के तापमान में कमी के साथ, बैटरी की क्षमता में काफी कमी आती है। बैटरी का उपयोग करते समय इसे ध्यान में रखा जाना चाहिए।
12 वी के विद्युत नेटवर्क में वोल्टेज वाले वाहनों पर, एक ही वोल्टेज की बैटरी स्थापित की जाती है, जिसमें छह बैटरी या दो बैटरी होती हैं, जिसमें 6 वी का वोल्टेज श्रृंखला में जुड़ा होता है। 24 वी के मुख्य वोल्टेज वाली कारों पर, उन्होंने श्रृंखला में जुड़े 12 वी के वोल्टेज के साथ दो बैटरी लगाई (एमएजेड -500, क्रेज़ -257)। मामले में जब स्टार्टर चालू होने पर केवल 24 वी के वोल्टेज का उपयोग किया जाता है, तो 12 वी के वोल्टेज के साथ दो बैटरी का उपयोग किया जाता है, समानांतर में जुड़ा हुआ है, उनके स्वचालित स्विचिंग के साथ सीरियल कनेक्शनइंजन शुरू होने के समय (MAZ-200, Kraz-214)। यात्री कारों पर, बैटरी आमतौर पर इंजन हुड के नीचे स्थित होती है। ट्रकों पर, बैटरी अक्सर ड्राइवर की सीट के नीचे या फ़ुटबोर्ड पर लगाई जाती है।
कारों के विद्युत उपकरण में सिंगल-वायर वायरिंग सिस्टम का उपयोग किया जाता है, जिसमें तारों में से एक कार के धातु के हिस्से, उसका द्रव्यमान होता है, इसलिए एक बैटरी टर्मिनल (आमतौर पर नकारात्मक) जमीन पर बंद होता है, और दूसरा ( सकारात्मक) नेटवर्क से जुड़ा है,
कुछ कार मॉडलों के लिए, नकारात्मक बैटरी टर्मिनल एक विशेष स्विच के माध्यम से जमीन से जुड़ा होता है। यह उपयोग में न होने पर बैटरी को मेन से डिस्कनेक्ट करने की अनुमति देता है, जो बैटरी को संभावित करंट लीकेज से बचाता है।
VB-318 प्रकार के स्विच के शरीर (चित्र 3) में एक बटन के साथ एक रॉड स्थापित है। रॉड के निचले सिरे पर, स्प्रिंग्स और एक सहायक संपर्क के साथ मुख्य गतिशील संपर्क होते हैं। चलती संपर्क आवास में तय किए गए निश्चित संपर्कों के ऊपर स्थित हैं। संपर्क जमीन से जुड़ा है, और अछूता संपर्क उस टर्मिनल से जुड़ा है जिससे तार बैटरी के नकारात्मक टर्मिनल से जुड़ा हुआ है। संपर्कों वाला तना स्प्रिंग्स द्वारा ऊपर की ओर दबाया जाता है। आवास के शीर्ष पर एक स्प्रिंग और एक छोटा बटन के साथ एक लॉकिंग प्लेट है।

चावल। 3. बैटरी स्विच
मुख्य बटन दबाकर बैटरी को नेटवर्क से जोड़ा जाता है। इस मामले में, स्थिर संपर्कों को पहले सहायक चलती संपर्क द्वारा बंद किया जाता है, और फिर मुख्य संपर्कों द्वारा, और बैटरी को जमीन से जोड़ा जाता है। इस मामले में, रॉड 6 को चालू स्थिति में लॉकिंग प्लेट 8 द्वारा तय किया जाता है, जो एक स्प्रिंग की क्रिया के तहत रॉड पर खांचे में प्रवेश करता है।
साइड बटन दबाकर बैटरी को बंद कर दिया जाता है, जो लॉकिंग प्लेट को शिफ्ट करता है और मुख्य रॉड को छोड़ता है। रॉड, संपर्कों के साथ उठकर, बैटरी सर्किट को खोलता है। श्रृंखला की कुछ गैर-एक साथ सहायक और मुख्य संपर्कों को बंद करने और खोलने से संपर्कों का जलना कम हो जाता है।
बैटरियों का एक निश्चित अंकन होता है (GOST 959-51 के अनुसार)। उदाहरण के लिए, GAZ-51A कार पर 3-ST-70-VD बैटरी लगाई गई है। पहली संख्या बैटरी में संचयकों (कोशिकाओं) की संख्या को इंगित करती है, और इसलिए कुल वोल्टेज, यह मानते हुए कि प्रत्येक सेल में 2 वी का वोल्टेज होता है। दूसरा नंबर आह में बैटरी की नाममात्र क्षमता को इंगित करता है। अक्षर CT इंगित करते हैं कि बैटरी एक चार्टर प्रकार है। टैंक की सामग्री को अक्षरों द्वारा दर्शाया गया है: ई - एबोनाइट, पी - एसिड-प्रतिरोधी आवेषण के साथ डामर-पिच द्रव्यमान, बी - एसिड-प्रतिरोधी आवेषण के बिना डामर-पिच द्रव्यमान। विभाजकों की सामग्री को अक्षरों द्वारा निर्दिष्ट किया जाता है: डी - लकड़ी, डीएस - लकड़ी और कांच लगा, एम - माइप्लास्ट, एमएस - माइप्लास्ट और ग्लास लगा, पी - मिपोर। अक्षर 3 का अर्थ है कि बैटरी ड्राई-चार्ज है।
उपयोग के लिए बैटरी तैयार करना
नई सूखी बैटरी को इलेक्ट्रोलाइट से भरा और चार्ज किया जाना चाहिए।
इलेक्ट्रोलाइट से तैयार किया जाता है बैटरी का अम्लऔर आसुत जल। इलेक्ट्रोलाइट तैयार करने के लिए, सल्फ्यूरिक एसिड की कार्रवाई के लिए प्रतिरोधी बर्तनों का उपयोग किया जाता है - सिरेमिक, इबोनाइट, ग्लास। आसुत जल पहले व्यंजन में डाला जाता है, और फिर एसिड सावधानी से और धीरे-धीरे जोड़ा जाता है।
बैटरी भरने के लिए इलेक्ट्रोलाइट का उपयोग बैटरी के प्रकार, जलवायु परिस्थितियों और मौसम के आधार पर एक निश्चित घनत्व (1.27-1.34) पर किया जाता है।
इलेक्ट्रोलाइट का आवश्यक घनत्व निर्माता के निर्देशों के अनुसार निर्धारित किया जाता है।
इलेक्ट्रोलाइट के घनत्व को एक विंदुक के साथ एक विशेष हाइड्रोमीटर से मापा जाता है।
बैटरी कोशिकाओं ^ में इलेक्ट्रोलाइट को विभाजकों के ऊपर स्थापित सुरक्षा कवच के ऊपर 10-15 मिमी के स्तर तक भरा जाना चाहिए। स्तर को एक ग्लास ट्यूब के साथ जांचा जाता है, जिसे सभी तरह से ढाल में उतारा जाता है, और ऊपरी छेद को बंद करके हटा दिया जाता है। ट्यूब में इलेक्ट्रोलाइट के कॉलम की ऊंचाई इसका स्तर निर्धारित करती है।
स्वचालित स्तर नियंत्रण वाली बैटरियों में, आपको प्लग को खोलना होगा और उन्हें पहले से पोंछे गए वेंटिलेशन फिटिंग पर रबर की झाड़ियों के साथ कसकर रखना होगा, फिर इलेक्ट्रोलाइट को कोशिकाओं में भराव गर्दन के ऊपरी किनारे के नीचे 15-20 मिमी के स्तर तक डालें। जब फिटिंग से प्लग हटा दिए जाते हैं, तो कोशिकाओं में इलेक्ट्रोलाइट सामान्य स्तर पर सेट हो जाएगा।
इलेक्ट्रोलाइट भरने के बाद 3-6 घंटे (बैटरी के प्रकार के आधार पर) के बाद, बैटरी के पॉजिटिव टर्मिनल को करंट सोर्स के पॉजिटिव पोल से और नेगेटिव टर्मिनल को नेगेटिव से जोड़कर चार्ज किया जाता है।
फ़ैक्टरी निर्देशों में निर्दिष्ट प्रत्येक प्रकार की बैटरी के लिए सामान्य वर्तमान में चार्जिंग की जाती है। चार्जिंग तब तक जारी रहती है जब तक कि बैटरी की सभी बैटरियों (कोशिकाओं) में विपुल गैस विकास (उबलना) न हो जाए, और इलेक्ट्रोलाइट का वोल्टेज और घनत्व 3 घंटे तक स्थिर रहता है।
चार्ज करते समय, सुनिश्चित करें कि इलेक्ट्रोलाइट का तापमान 45 डिग्री सेल्सियस से ऊपर नहीं बढ़ता है।
पहले चार्ज के अंत तक, इलेक्ट्रोलाइट के घनत्व की जाँच की जाती है, और यदि आवश्यक हो, तो इसे सभी कोशिकाओं में सामान्य में लाया जाता है, जिसके लिए इलेक्ट्रोलाइट के किस हिस्से को रबर के बल्ब के साथ सेल से बाहर निकाला जाता है और डिस्टिल्ड के साथ टॉप किया जाता है। पानी या बढ़े हुए घनत्व का इलेक्ट्रोलाइट।
पहले चार्ज के बाद, नई बैटरियों को सेवा में लगाया जा सकता है। ऑपरेशन के दौरान बैटरी के जीवन का विस्तार करने के लिए, कई चार्जिंग चक्रों को पूरा करना उपयोगी होता है, जब तक कि एक सेल का वोल्टेज 1.7 V तक गिर नहीं जाता, तब तक नाममात्र डिस्चार्ज करंट के साथ चार्ज करने के बाद बैटरी को डिस्चार्ज करना।
बैटरी की देखभाल और समस्या निवारण
देखभाल के प्रमुख तत्वों में शामिल हैं:
1) फास्टनरों की जाँच करना और बैटरी की सफाई करना;
2) टर्मिनलों की सफाई और कसना;
3) इलेक्ट्रोलाइट स्तर की जाँच करना और उसे ऊपर उठाना;
4) बैटरी के चार्ज की डिग्री की जाँच करना;
5) चार्जिंग करंट की जाँच करना;
6) तेजी से डिस्चार्ज और शॉर्ट सर्किट से बैटरी की सुरक्षा।
बैटरी की क्षति से बचने के लिए बैटरी फास्टनरों की जाँच करना आवश्यक है।
ढीले फास्टनरों के साथ मिलाने से। सॉकेट में बैटरी का बन्धन कड़ा होना चाहिए। ट्रकों पर, बैटरी के नीचे रबर के गास्केट लगाए जाने चाहिए। समय-समय पर, मोनोब्लॉक में दरारें और उसमें से इलेक्ट्रोलाइट के रिसाव की जांच करना आवश्यक है। आपको ढक्कन पर भरने वाले मैस्टिक की अखंडता की भी जांच करनी चाहिए।
बैटरी की दूषित सतह पर बैटरी (कोशिकाओं) के शॉर्ट सर्किट को खत्म करने के लिए बैटरी को साफ करने की आवश्यकता होती है, आमतौर पर इलेक्ट्रोलाइट को छिड़क कर गीला किया जाता है। बैटरी की सतह को साफ कपड़े से साफ करना चाहिए। बैटरी की सतह पर गिराए गए इलेक्ट्रोलाइट को अमोनिया या सोडा ऐश (10% घोल) के घोल में भिगोकर साफ कपड़े से पोंछना चाहिए। जार में जमा होने वाली गैसों से होने वाले नुकसान को रोकने के लिए वेंटिलेशन छेद को भी साफ किया जाना चाहिए।
टर्मिनलों पर अच्छा संपर्क सुनिश्चित करने के लिए टर्मिनलों की सफाई और कसना आवश्यक है। टर्मिनलों को अच्छी तरह से साफ किया जाना चाहिए, कसकर कड़ा किया जाना चाहिए और उनके ऑक्सीकरण को रोकने के लिए तकनीकी वैसलीन या ग्रीस की एक पतली परत के साथ बाहर से चिकनाई की जानी चाहिए। तार बन्धन को द्रव्यमान तक कसने के लिए भी आवश्यक है। तारों पर मजबूत तनाव की अनुमति न दें, क्योंकि इससे आउटपुट टर्मिनलों को नुकसान हो सकता है और मैस्टिक में दरारें बन सकती हैं।
इलेक्ट्रोलाइट स्तर की जाँच आवश्यक है क्योंकि इलेक्ट्रोलाइट के वाष्पीकरण और उबलने के परिणामस्वरूप इलेक्ट्रोलाइट स्तर गिर सकता है। जब इलेक्ट्रोलाइट का स्तर कम हो जाता है, तो बैटरी बैंकों में आसुत जल डाला जाता है, क्योंकि केवल पानी उबलता है।
समय-समय पर पूरी तरह चार्ज बैटरी के साथ इलेक्ट्रोलाइट के घनत्व की जांच करें और सुनिश्चित करें कि यह सभी बैंकों में समान है, यदि आवश्यक हो, तो इलेक्ट्रोलाइट का घनत्व सामान्य हो जाता है।
बैटरी के डिस्चार्ज की डिग्री को इलेक्ट्रोलाइट के घनत्व या वोल्टमीटर का उपयोग करके जांचा जा सकता है लोड कांटा.
बैटरी हमेशा चार्ज अवस्था में होनी चाहिए। यदि परीक्षण के दौरान बैटरी अपूर्ण रूप से चार्ज हो जाती है, तो बैटरी के सामान्य संचालन को बाधित करने वाले कारणों को स्थापित करते हुए, इसे चार्ज करने के उपाय करना आवश्यक है।
एक बैटरी जो सर्दियों में 25% से अधिक डिस्चार्ज हो जाती है और गर्मियों में 50% से अधिक डिस्चार्ज हो जाती है, उसे हटाकर रिचार्ज करना चाहिए।
यदि बैटरी लंबे समय तक पूरी तरह से चार्ज नहीं होती है, तो इससे इसकी प्लेटों को नुकसान होता है। पर सर्दियों का समयडिस्चार्ज की गई बैटरी में इलेक्ट्रोलाइट बैटरी को फ्रीज और नष्ट कर सकता है।
चार्जिंग करंट और बैटरी चार्जिंग मोड का नियंत्रण वाहन के इलेक्ट्रिकल सिस्टम में उपलब्ध एमीटर की रीडिंग के अनुसार मोटे तौर पर किया जा सकता है।
यदि बैटरी चार्ज की जाती है, तो इंजन क्रैंकशाफ्ट के क्रांतियों की संख्या में वृद्धि पर भी एमीटर सुई लगभग मध्य स्थिति से विचलित नहीं होती है। जब बैटरी को डिस्चार्ज किया जाता है, तो इंजन शाफ्ट के क्रांतियों की संख्या में वृद्धि की स्थिति में, बैटरी को चार्ज करने के लिए उपयोग किए जाने वाले करंट में वृद्धि के कारण एमीटर सुई चार्जिंग करंट की दिशा में महत्वपूर्ण रूप से विचलित हो जाती है। जब कार विपरीत दिशा में चल रही हो या चेतावनी प्रकाश चालू हो तो एमीटर सुई का विचलन इंगित करता है कि बैटरी कम है।
प्लेटों के ताना-बाना और सक्रिय द्रव्यमान के छिलने से बचने के लिए बैटरी को तेजी से डिस्चार्ज और शॉर्ट सर्किट से बचाना आवश्यक है। इसलिए, स्टार्टर को चालू करने के लिए लंबे समय तक और लगातार कई बार असंभव है, जो एक बहुत मजबूत वर्तमान की खपत करता है। सर्दियों में कम तापमान पर स्टार्टर के साथ बहुत ठंडा इंजन शुरू करने की अनुशंसा नहीं की जाती है। इंजन को पहले से गरम करना और क्रैंकशाफ्ट को कई बार मैन्युअल रूप से चालू करना आवश्यक है।
बैटरी का निरीक्षण करते समय, उसमें खुली आग न लगाएं, क्योंकि इलेक्ट्रोलाइट के ऊपर गैसों का एक फ्लैश हो सकता है।
गर्मियों से सर्दियों के संचालन में या इसके विपरीत स्विच करते समय, इलेक्ट्रोलाइट के घनत्व को अनुशंसित मूल्य पर लाना आवश्यक है।
सर्दियों में, खुली बैटरी को इन्सुलेट किया जाना चाहिए।
कार पर बैटरी स्थापित करते समय, इसके टर्मिनलों को जमीन और सर्किट से सही ढंग से जोड़ना आवश्यक है। सही कनेक्शन को एमीटर से जांचा जा सकता है। जब बैटरी डिस्चार्ज हो जाती है, तो तीर को उचित दिशा में (धन चिह्न की ओर) विचलन करना चाहिए। बैटरी टर्मिनलों की ध्रुवता टर्मिनलों पर प्लस और माइनस संकेतों द्वारा निर्धारित की जा सकती है, और उनकी अनुपस्थिति में, टर्मिनलों से अम्लीय पानी में तारों को कम करके या कच्चे आलू का उपयोग करके। अम्लीय पानी में, ऋणात्मक (ऋणात्मक) तार पर, गैस के बुलबुले तेजी से निकलते हैं, और आलू में फंसे धनात्मक (प्लस) तार के चारों ओर एक हरा धब्बा दिखाई देगा।
बैटरी भंडारण। यदि बैटरी को कार से हटा दिया जाता है और अपेक्षाकृत कम भंडारण में रखा जाता है, तो इसे पहले पूरी तरह से चार्ज किया जाना चाहिए, इलेक्ट्रोलाइट स्तर की जांच करें, इलेक्ट्रोलाइट के घनत्व को सामान्य मान पर लाएं (15 डिग्री सेल्सियस पर 1.280 से अधिक नहीं), अच्छी तरह से मोनोब्लॉक और कवर के बाहरी हिस्से को पोंछकर साफ करें, टर्मिनलों को साफ करें और एक साफ हवादार कमरे में एक स्थिर तापमान पर रखें।
आंतरिक स्व-निर्वहन से बचने और सकारात्मक प्लेटों के बढ़ते क्षरण को खत्म करने के लिए, इलेक्ट्रोलाइट के साथ बैटरी को ठंडे कमरे में -25 डिग्री सेल्सियस से कम और 0 डिग्री सेल्सियस से अधिक नहीं के निरंतर तापमान पर स्टोर करना बेहतर होता है। ऐसी स्थितियों में बैटरियों का भंडारण करते समय, मासिक रूप से इलेक्ट्रोलाइट घनत्व की जांच करना आवश्यक है, बैटरी को केवल तभी रिचार्ज करना जब घनत्व अनुमेय मान (1.230 से नीचे 15 डिग्री सेल्सियस) से नीचे चला जाता है। भंडारण की इस पद्धति के साथ बैटरियों की सामान्य स्थिति में, उन्हें संचालन में लगाने से पहले ही उन्हें चार्ज करना आवश्यक है।
जब बैटरियों को 0°C से ऊपर के तापमान पर संग्रहीत किया जाता है, तो उन्हें स्वयं-निर्वहन के कारण खोई हुई क्षमता को बहाल करने के लिए मासिक रूप से चार्ज किया जाना चाहिए।
इन भंडारण विधियों के साथ, बैटरियों को हमेशा उपयोग के लिए तैयार किया जाता है।
लंबी अवधि के भंडारण के साथ, उदाहरण के लिए, छह महीने से अधिक, और अगर बैटरी को बार-बार रिचार्ज करना असंभव है, जो पहली भंडारण विधि के दौरान आवश्यक है, तो इलेक्ट्रोलाइट के बिना बैटरी को स्टोर करने की एक विधि का अभ्यास किया जाता है। इस मामले में, बैटरी को क्षमता के 1/20 के अनुरूप करंट के साथ पूरी तरह से डिस्चार्ज किया जाना चाहिए, जब तक कि एक बैटरी पर वोल्टेज 1.7 V तक गिर न जाए, फिर, बैटरी निकालने के बाद, उसमें से इलेक्ट्रोलाइट डालें और डिब्बे को कुल्ला करें। आसुत जल के साथ अच्छी तरह से। रिंसिंग तब तक की जानी चाहिए जब तक कि पानी ऑक्सीकरण करना बंद न कर दे। बैटरी को धोने और अच्छी तरह से सुखाने के बाद, इसके डिब्बे के छिद्रों को कसकर बंद करना और बाहर की सफाई करना और बैटरी को लंबे समय तक भंडारण के लिए इस रूप में रखना आवश्यक है।
बैटरी दोष। बैटरी के मुख्य दोष हैं: अपर्याप्त चार्ज, ओवरचार्जिंग, प्लेट सल्फेशन, क्षमता में कमी, आंतरिक स्व-निर्वहन, प्लेट वारपिंग, बैटरी रिसाव।
कम चार्जिंग करंट, तारों के खराब बन्धन और टर्मिनलों के ऑक्सीकरण, इंजन के नहीं चलने पर रिसाव या उच्च करंट खपत, स्टार्टर के अयोग्य उपयोग के कारण अपर्याप्त बैटरी चार्ज प्राप्त होता है। अपर्याप्त आवेशित धाराहो सकता है जब रिले-रेगुलेटर गलत तरीके से समायोजित किया गया हो या जनरेटर ठीक से काम नहीं कर रहा हो। अपर्याप्त बैटरी चार्ज के संकेत इसमें कम इलेक्ट्रोलाइट घनत्व और अपर्याप्त बैटरी वोल्टेज हैं।
बैटरी को रिचार्ज करना तब होता है जब रिले-रेगुलेटर के अनुचित समायोजन के कारण चार्जिंग करंट अत्यधिक मजबूत होता है। ओवरचार्जिंग का संकेत इलेक्ट्रोलाइट का बार-बार उबलना और इसके स्तर में तेजी से कमी है।
प्लेटों का सल्फेशन यह है कि प्लेटों को एक सफेद क्रिस्टलीय कोटिंग के साथ कवर किया जाता है, जिससे विद्युत प्रवाह के पारित होने और प्लेटों के सक्रिय द्रव्यमान में इलेक्ट्रोलाइट के प्रवेश को मुश्किल हो जाता है। नतीजतन, रासायनिक प्रक्रियाएं धीमी हो जाती हैं और बैटरी की क्षमता कम हो जाती है।
सल्फेशन का एक बाहरी संकेत बढ़ते भार के साथ बैटरी वोल्टेज में तेज गिरावट है। उदाहरण के लिए, स्टार्टर या सिग्नल को चालू करते समय प्रकाश बल्ब, जो काफी चमकीला जलता है, लगभग बाहर चला जाता है। लोड प्लग के साथ सल्फेशन से गुजरने वाली बैटरी कोशिकाओं की जांच करते समय, कोशिकाओं के ध्रुवों पर वोल्टेज तेजी से कम हो जाता है।
सल्फेशन बैटरी के गंभीर रूप से डिस्चार्ज होने या अपूर्ण रूप से चार्ज होने की स्थिति में इसके लंबे समय तक संचालन के परिणामस्वरूप होता है। बैटरियों को सल्फेशन से बचाने के लिए, उन्हें चार्ज अवस्था में व्यवस्थित रूप से मॉनिटर करना और बनाए रखना आवश्यक है, साथ ही चार्जिंग स्टेशन पर समय-समय पर नियंत्रण और प्रशिक्षण चक्र आयोजित करना आवश्यक है। मजबूत सल्फेशन के कारण, बैटरी प्लेटें विफल हो जाती हैं और उन्हें मरम्मत और बहाल नहीं किया जा सकता है।
धारिता में कमी कमी के कारण होती है काम की सतहप्लेटों के सक्रिय द्रव्यमान के छिलने या इलेक्ट्रोलाइट स्तर में कमी के कारण प्लेटें। क्षमता में कमी का संकेत चार्जिंग के दौरान इलेक्ट्रोलाइट का तेजी से उबलना है, इसके घनत्व में मामूली वृद्धि के साथ-साथ तेजी से निर्वहनऑपरेशन के दौरान बैटरी। सक्रिय द्रव्यमान की स्पैलिंग बैटरी के एक मजबूत ओवरचार्जिंग के परिणामस्वरूप प्राप्त की जाती है या जब बैटरी को एक बड़े प्रवाह के साथ छुट्टी दे दी जाती है, उदाहरण के लिए, स्टार्टर का लंबे समय तक उपयोग करते समय।
बैटरी का आंतरिक स्व-निर्वहन तब होता है जब इलेक्ट्रोलाइट के लिए आसुत जल का उपयोग किया जाता है। खराबी का एक लक्षण एक गैर-काम करने वाली बैटरी का भी तेजी से निर्वहन है। इस खराबी को खत्म करने के लिए, बैटरी को डिस्चार्ज किया जाता है और आसुत जल से अच्छी तरह से धोया जाता है, इसके बाद इसे उचित गुणवत्ता और घनत्व और चार्जिंग के इलेक्ट्रोलाइट से भर दिया जाता है।
बहुत अधिक घनत्व वाले इलेक्ट्रोलाइट के उपयोग के कारण लकड़ी के विभाजकों के नष्ट होने के कारण बैटरी कोशिकाओं के अंदर एक शॉर्ट सर्किट होता है। इस मामले में, गिरने वाला सक्रिय द्रव्यमान प्लेटों को बंद कर देता है। बैटरी के आंतरिक शॉर्ट सर्किट के साथ, इसका वोल्टेज जल्दी कम हो जाता है, इलेक्ट्रोलाइट का घनत्व और बैटरी की क्षमता कम हो जाती है।
लंबे समय तक स्टार्टर का उपयोग करने और सर्किट में शॉर्ट सर्किट के मामले में अत्यधिक डिस्चार्ज करंट के साथ प्लेटों का ताना-बाना प्राप्त होता है। इस मामले में, बैटरी विफल हो जाती है।
प्रतिश्रेणी: - कार विद्युत उपकरण
कोई फर्क नहीं पड़ता कि आप लेख का शीर्षक कैसे तैयार करते हैं, यह अभी भी सही होगा। बैटरी के डिजाइन में रसायन और ऊर्जा एक साथ बंधे होते हैं।
लीड-एसिड बैटरी कई वर्षों तक चार्ज-डिस्चार्ज मोड में काम कर सकती हैं। वे जल्दी से रिचार्ज करते हैं और संग्रहीत ऊर्जा को जल्दी से छोड़ते हैं। इन कायांतरणों का रहस्य रसायन शास्त्र में है, क्योंकि यह वह है जो बिजली को परिवर्तित करने में मदद करती है, लेकिन कैसे?
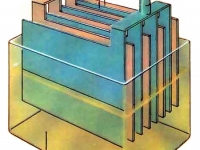 बैटरी में ऊर्जा रूपांतरण का "रहस्य" अभिकर्मकों के एक सेट द्वारा प्रदान किया जाता है, जिसमें एक ऑक्सीकरण एजेंट और एक इलेक्ट्रोलाइट के माध्यम से बातचीत करने वाला एक कम करने वाला एजेंट होता है। कम करने वाले एजेंट (स्पंजी लेड Pb) पर ऋणात्मक आवेश होता है। एक रासायनिक प्रतिक्रिया के दौरान, यह ऑक्सीकरण करता है, और इसके इलेक्ट्रॉन ऑक्सीकरण एजेंट की यात्रा करते हैं, जिसका सकारात्मक चार्ज होता है। ऑक्सीकरण एजेंट (सीसा डाइऑक्साइड PbO2) कम हो जाता है, और परिणाम एक विद्युत प्रवाह होता है।
बैटरी में ऊर्जा रूपांतरण का "रहस्य" अभिकर्मकों के एक सेट द्वारा प्रदान किया जाता है, जिसमें एक ऑक्सीकरण एजेंट और एक इलेक्ट्रोलाइट के माध्यम से बातचीत करने वाला एक कम करने वाला एजेंट होता है। कम करने वाले एजेंट (स्पंजी लेड Pb) पर ऋणात्मक आवेश होता है। एक रासायनिक प्रतिक्रिया के दौरान, यह ऑक्सीकरण करता है, और इसके इलेक्ट्रॉन ऑक्सीकरण एजेंट की यात्रा करते हैं, जिसका सकारात्मक चार्ज होता है। ऑक्सीकरण एजेंट (सीसा डाइऑक्साइड PbO2) कम हो जाता है, और परिणाम एक विद्युत प्रवाह होता है।
इलेक्ट्रोलाइट एक तरल है जो वर्तमान का एक खराब कंडक्टर है, लेकिन आयनों के लिए एक अच्छा कंडक्टर है। यह सल्फ्यूरिक एसिड (H2SO4) का एक जलीय घोल है। एक रासायनिक प्रतिक्रिया में, एक प्रक्रिया होती है जो स्कूल से सभी को ज्ञात होती है - इलेक्ट्रोलाइटिक पृथक्करण।
प्रतिक्रिया के दौरान, - धनात्मक आवेशित आयन (H+) धनात्मक इलेक्ट्रोड को भेजे जाते हैं, और ऋणात्मक आवेशित आयन (SO42-) ऋणात्मक को। जब बैटरी को डिस्चार्ज किया जाता है, तो कम करने वाले एजेंट (स्पंजी लेड) से, इलेक्ट्रोलाइट के माध्यम से सकारात्मक इलेक्ट्रोड में, Pb2 + के सकारात्मक चार्ज वाले आयन भेजे जाते हैं।
चतुर्भुज लेड आयन (Pb4+) द्विसंयोजी आयनों (Pb4+) में परिवर्तित हो जाते हैं। हालांकि, यह सभी रासायनिक प्रतिक्रियाएं नहीं हैं। जब ऋणात्मक आवेश (SO42-) के साथ अम्लीय अवशेषों के आयन धनात्मक आवेशित लेड आयनों (Pb2+) के साथ जुड़ते हैं, तो दोनों इलेक्ट्रोड पर लेड सल्फेट (PbSO4) बनता है। लेकिन यह बैटरी के लिए पहले से ही खराब है। सल्फेशन बैटरी जीवन को छोटा करता है और समय के साथ जमा हो सकता है, जिससे बैटरी खराब हो सकती है। खराब असरपारंपरिक लेड-एसिड बैटरी में रासायनिक प्रतिक्रियाएं गैसें होती हैं।

क्या होता है जब बैटरी को रिचार्ज किया जाता है?
इलेक्ट्रॉनों को एक नकारात्मक चार्ज के साथ एक इलेक्ट्रोड में भेजा जाता है, जहां वे अपना कार्य करते हैं - वे लीड आयनों (Pb2+) को बेअसर करते हैं। बैटरियों में होने वाली रासायनिक प्रतिक्रियाओं को निम्नलिखित सूत्र द्वारा वर्णित किया जा सकता है:
इलेक्ट्रोलाइट का घनत्व और बैटरी में इसका स्तर इस बात पर निर्भर करता है कि बैटरी चार्ज है या डिस्चार्ज। इलेक्ट्रोलाइट घनत्व में परिवर्तन निम्न सूत्र द्वारा वर्णित किया जा सकता है:
![]()
जहां बैटरी डिस्चार्ज दर, जिसे प्रतिशत के रूप में मापा जाता है, Cp है। पूरी तरह चार्ज होने पर इलेक्ट्रोलाइट का घनत्व Rz होता है। पूर्ण निर्वहन पर इलेक्ट्रोलाइट घनत्व - पीपीआर।
मानक तापमान जिस पर माप किए जाते हैं वह + 25 डिग्री सेल्सियस है, तापमान के अनुसार इलेक्ट्रोलाइट का घनत्व + 25 डिग्री सेल्सियस, जी / सेमी 3 - पी 25 है।
एक रासायनिक प्रतिक्रिया के दौरान, सकारात्मक इलेक्ट्रोड नकारात्मक इलेक्ट्रोड की तुलना में 1.6 गुना अधिक एसिड का उपयोग करते हैं। जब बैटरी को डिस्चार्ज किया जाता है, तो इलेक्ट्रोलाइट की मात्रा बढ़ जाती है, और जब इसे चार्ज किया जाता है, तो इसके विपरीत, यह घट जाती है।
इस तरह, रासायनिक प्रतिक्रियाओं की मदद से, बैटरी प्राप्त करती है और फिर विद्युत ऊर्जा छोड़ती है।
मैंने गलती से इस पर टिप्पणियों के साथ देखा, और एसिड (आम लोगों में सीसा) बैटरी के क्षेत्र में लोगों की निरक्षरता के बारे में मुझमें इतना गुस्सा उबल रहा था, कि मैं इसे बर्दाश्त नहीं कर सका और "गीक्स" को लिखने का फैसला किया ( एक गीक होने के लिए, जैसा कि यह पता चला है, यह एक महंगा फोन खरीदने के लिए पर्याप्त नहीं है) एक छोटा बैटरी लेख। उन गलतियों को ध्यान में रखते हुए जो मेरी आँखों को लगातार विलंबित करती हैं और उन्हें ठीक करने की एक धार्मिक इच्छा पैदा करती हैं।
आइए शीर्षक से शुरू करते हैं। मैं अक्सर देखता हूं कि तीन अक्षर A-K-Bवे वह सब कुछ कहते हैं जिसे चार्ज किया जा सकता है, बिल्कुल कोई भी बैटरी। विशेष रूप से तीन अक्षर वाले लोग Li-ion बैटरी को कॉल करना पसंद करते हैं। वास्तव में, बैटरी रिचार्जेबल एसिड बैटरी का संक्षिप्त नाम है। उनका मतलब केवल एक प्रकार की बैटरी है - लेड एसिड। आधुनिक दृष्टिकोण से, यह नाम कुछ संज्ञानात्मक असंगति का कारण बनता है। फिलहाल, "बैटरी" शब्द का अर्थ है। एक गैल्वेनिक सेल जिसे चार्ज नहीं किया जा सकता उसे "बैटरी" शब्द में बदल दिया गया था। और यह पता चला है, जैसे कि "रिचार्जेबल" शब्द के कारण, यह एक बैटरी है जिसे चार्ज किया जा सकता है, लेकिन "बैटरी" शब्द के कारण, यह एक बैटरी की तरह है जिसे चार्ज नहीं किया जा सकता है। वास्तव में, बैटरी केवल गैल्वेनिक कोशिकाओं की एक श्रृंखला होती है और "बैटरी" शब्द के साथ केवल एक सामान्य जड़ होती है।
इसके बाद, आइए कुछ मिथकों पर चलते हैं, अर्थात् मुख्य मिथक - एक कार के लिए एक बैटरी में यूपीएस के लिए बैटरी से कुछ महत्वपूर्ण अंतर होते हैं। और आप उन्हें इधर-उधर इस्तेमाल नहीं कर सकते।
रासायनिक दृष्टिकोण से, कोई भी बैटरी ठीक वैसा. उन्हें कैसे व्यवस्थित किया जाता है? बहुत संक्षेप में - यदि बैटरी चार्ज की जाती है, तो एक इलेक्ट्रोड एक लीड ग्रिड होता है जिस पर PbO 2 पेस्ट लगाया जाता है, दूसरा वही ग्रिड होता है जिसमें स्पंजी लेड पेस्ट होता है। इलेक्ट्रोलाइट सल्फ्यूरिक एसिड का एक समाधान है। निर्वहन के दौरान, PbO2 कम हो जाता है और सल्फ्यूरिक एसिड के साथ परस्पर क्रिया करके PbSO 4 बनाता है। दूसरे इलेक्ट्रोड पर लेड ऑक्सीकरण करता है और फिर से PbSO 4 बनाता है। डिस्चार्ज के अंत में हमारे पास दोनों जाली प्लेट्स (अधिक या कम) लेड सल्फेट से भरी होती हैं। जब बैटरी को चार्ज किया जाता है, तो इलेक्ट्रोलिसिस होता है और लेड सल्फेट फिर से डाइऑक्साइड और धात्विक लेड में बनता है। बेशक, यहां इस बात पर जोर दिया जाना चाहिए कि इलेक्ट्रोड समान नहीं हैं और उनकी ध्रुवीयता भ्रमित नहीं होनी चाहिए। यहां तक कि उत्पादन के स्तर पर भी, उपयुक्त एडिटिव्स को उनके परिचालन गुणों में सुधार के लिए इलेक्ट्रोड की कोटिंग में पेश किया जाता है। उसी समय, एक इलेक्ट्रोड के लिए उपयोगी योजक दूसरे के लिए हानिकारक होते हैं। बहुत पुराने समय में, कहीं पिछली सदी की शुरुआत में, परिस्थितियों में साधारण बैटरी, गलती से या किसी उद्देश्य के लिए बैटरी को उल्टा करना संभव था और उसके बाद कुछ समय के लिए यह काम करता था। मुझे संदेह है कि अब इसकी अनुमति है।
12V बैटरी में 6 ऐसे सेल होते हैं, 6V बैटरी में 3। आदि। कई बैटरियों पर वोल्टेज के मूल्य से गुमराह होते हैं। इसके अलावा, नाममात्र वोल्टेज, चार्ज, डिस्चार्ज के मूल्य। एक ओर, बैटरी को 12V कहा जाता है (और 6V, 24V भी उपलब्ध हैं, मेरी राय में, कभी-कभी 4V भी पाए जाते हैं), लेकिन समान UPS बैटरी के मामले में, निर्माता 13.5V से ऊपर के वोल्टेज का संकेत देता है।
उदाहरण के लिए:
यहां हम देखते हैं कि मजबूर मोड में, वोल्टेज शुल्कशायद 15V जितना।
बैटरी पर वोल्टेज वक्र द्वारा सब कुछ समझाया जाएगा:

बाईं ओर हम 12 कोशिकाओं (24V नाममात्र), 6 कोशिकाओं (12V नाममात्र) की बैटरी के लिए वोल्टेज देखते हैं, और सबसे उपयोगी, एक सेल के लिए। डिस्चार्ज / चार्ज के दौरान अवांछनीय वोल्टेज के चिह्नित क्षेत्र भी हैं। वक्र से हम निष्कर्ष निकाल सकते हैं:
1 वोल्टेज 12 वी, 24 वी, आदि। नाममात्र हैं और केवल बैटरी में गैल्वेनिक कोशिकाओं की संख्या (दो से विभाजित करके) इंगित करते हैं। यह सुविधा के लिए सिर्फ एक नाम है।
2 चार्जिंग वोल्टेज 2.5V/सेल तक पहुंच सकता है, जो 12V बैटरी के लिए 15V से मेल खाती है।
3 चार्ज की गई बैटरी का वोल्टेज 2.1-2.2 V / सेल के मान पर स्वीकार्य माना जाता है, जो कि 12V बैटरी के लिए 12.6-13.2V से मेल खाती है।
सैद्धांतिक रूप से, बैटरी को 2.4 वी/सेल या उससे भी थोड़ा अधिक के मूल्यों पर चार्ज किया जा सकता है, हालांकि, इस तरह की चार्जिंग इलेक्ट्रोड की स्थिति और इलेक्ट्रोलाइट एकाग्रता दोनों को नकारात्मक रूप से प्रभावित करेगी। एक बार, स्क्रैप करने से पहले, मैंने लगभग 12V की बैटरी को लगभग वोल्टेज में आसानी से चार्ज किया। 14.5V (मुझे अब सटीक मान याद नहीं है)।
इसलिए, जिस लेख से मैंने शुरुआत की, उसके लेखक ने फैसला किया कि कार की बैटरी का चार्ज वोल्टेज और यूपीएस की बैटरी अलग-अलग हैं। यह सच नहीं है, उनके पास एक ही प्रकार के इलेक्ट्रोड होते हैं और इलेक्ट्रोलाइट में सल्फ्यूरिक एसिड की समान सांद्रता होती है (प्रायोगिक रूप से प्रदान करने के लिए बहुत पहले चयनित) अधिकतम वोल्टेजऔर न्यूनतम स्व-निर्वहन)। हालाँकि, बैटरी में क्या होता है, इसे बहुत अधिक वोल्टेज मान पर चार्ज क्यों नहीं किया जा सकता है?
में क्यों कार बैटरीआपको पानी जोड़ने की आवश्यकता है, लेकिन आपको यूपीएस से बैटरी की आवश्यकता नहीं है? ये प्रश्न हमें पानी के अपघटन के तनाव के क्षेत्र में आसानी से जाने की अनुमति देते हैं। जैसा कि मैंने ऊपर लिखा है, जब बैटरी चार्ज होती है, तो इलेक्ट्रोलिसिस होता है। हालाँकि, PbSO 4 को PbO 2 और Pb में बदलने पर पूरा करंट खर्च नहीं होता है। वर्तमान का एक हिस्सा अनिवार्य रूप से पानी के अपघटन पर खर्च किया जाएगा, जो इलेक्ट्रोलाइट का एक महत्वपूर्ण हिस्सा बनाता है:
2एच 2 ओ \u003d 2एच 2 + ओ 2
सैद्धांतिक गणना लगभग इस प्रतिक्रिया के लिए वोल्टेज मान देती है। 1.2 वी। मैं आपको याद दिलाता हूं कि चार्ज करते समय सेल पर वोल्टेज स्पष्ट रूप से 2V से अधिक होता है। सौभाग्य से, पानी केवल 2V से ऊपर सक्रिय रूप से विघटित होना शुरू होता है, और उद्योग में, इससे हाइड्रोजन और ऑक्सीजन प्राप्त करने के लिए, प्रक्रिया 2.1-2.6V (ऊंचे तापमान पर) पर की जाती है। जैसा भी हो, यहां हम इस निष्कर्ष पर पहुंचे हैं कि बैटरी चार्जिंग प्रक्रिया के अंत में होगा अनिवार्य रूप सेइलेक्ट्रोलाइट में पानी के तत्वों में अपघटन की प्रक्रिया। परिणामी ऑक्सीजन और हाइड्रोजन केवल प्रतिक्रिया क्षेत्र से बच जाते हैं। उनके बारे में निम्नलिखित मिथक हैं:
1. हाइड्रोजन अत्यंत विस्फोटक है! बैटरी को रिचार्ज करें और कम से कम उस कमरे को खो दें जहां वह था!
वास्तव में, इलेक्ट्रोलिसिस के दौरान जारी हाइड्रोजन की मात्रा कमरे के आयतन की तुलना में नगण्य है। हवा में 4% की सांद्रता में हाइड्रोजन का विस्फोट होता है। यदि हम मान लें कि इलेक्ट्रोलिसिस 3*3*3 मीटर या 27 क्यूबिक मीटर वाले कमरे में किया जाता है, तो हमें कमरे को 27*0.04=1.1 क्यूबिक मीटर से भरना होगा। हाइड्रोजन। H2 की इतनी मात्रा प्राप्त करने के लिए, लगभग पूरी तरह से विघटित होना आवश्यक होगा। 49 मोल पानी या इसकी 884 ग्राम। अगर किसी ने इलेक्ट्रोलिसिस देखा है, तो वे समझेंगे कि यह कितना है। या चलो समय के साथ आगे बढ़ने की कोशिश करते हैं। 6A की बड़ी बैटरी के लिए एक मानक चार्ज करंट के साथ, फैराडे समीकरण हाइड्रोजन की इस मात्रा को 437 घंटे या 18.2 दिनों के उत्पादन के लिए आवश्यक समय देता है। हाइड्रोजन के साथ एक विस्फोटक एकाग्रता के साथ एक कमरा भरने के लिए, आपको ढाई सप्ताह तक चार्ज करने के बारे में भूलना होगा! लेकिन अगर ऐसा होता भी है, तो सल्फ्यूरिक एसिड की सांद्रता तब तक बढ़ जाएगी जब तक कि इसका घोल 12V चार्ज के लिए बहुत अधिक प्रतिरोध प्राप्त नहीं कर लेता और करंट नगण्य हो जाता है। हां, और हाइड्रोजन बस वाष्पित हो जाएगा।
बहुत कम ही, बड़ी बैटरियों के मामलों में सीधे विस्फोट इस तथ्य के कारण होता है कि मुक्त हाइड्रोजन, किसी कारण से, संलग्न स्थान को नहीं छोड़ सकता है। लेकिन इस मामले में भी, कुछ भी भयानक नहीं होता है - अक्सर विस्फोट केवल मामले के ऊपरी हिस्से के मामूली विरूपण के लिए पर्याप्त होता है, लेकिन मुख्य कनेक्शन को तोड़ने के लिए नहीं। और इस तरह के नुकसान के बाद भी बैटरी आगे भी काम कर सकती है।
2. इलेक्ट्रोलिसिस के दौरान, घातक जहरीला और हाइड्रोजन से कम विस्फोटक नहीं, हाइड्रोजन सल्फाइड बन सकता है!
हमारा नहीं, समय-समय पर अंग्रेजी भाषा की पोस्ट में एक मिथक आया। सैद्धांतिक रूप से, निश्चित रूप से, इतने बड़े वोल्टेज को लागू करना और इस प्रकार बनाना संभव है। इतना बड़ा करंट कि कैथोड पर सल्फेट आयन के अपचयन की प्रक्रिया शुरू हो जाएगी। इसके लिए वोल्टेज पर्याप्त होगा, और कमी उत्पादों के पास इलेक्ट्रोड से दूर फैलने का समय नहीं होगा, और कमी जारी रहेगी। लेकिन एक दर्जन या तीन वोल्ट के भीतर और 6A की वर्तमान सीमा के साथ चार्ज करना शायद ही इसके लिए सक्षम हो। एक बार, मैंने सल्फेट को SO 2 तक कम करने की प्रक्रिया देखी, हाँ, यह संभव है; प्रयोग के दौरान सहपाठियों ने गलती से कुछ गलत कर दिया। लेकिन यह एक दुर्लभ वस्तु है। वहां, सल्फ्यूरिक एसिड की सांद्रता बैटरी में उपयोग की तुलना में काफी अधिक थी, इलेक्ट्रोड और इसकी अन्य सामग्री का एक अलग डिजाइन था, और निश्चित रूप से, वोल्टेज और वर्तमान ताकत अत्यधिक थी। और SO 2, H 2 S नहीं है।
3. इलेक्ट्रोलिसिस के दौरान जाली सामग्री से आर्सेनिक और सुरमा जहरीली आर्सिन और स्टाइबाइन में कम हो जाएगा!
वास्तव में, झंझरी में अपेक्षाकृत अधिक मात्रा में सुरमा होता है, और आधुनिक झंझरी में शायद आर्सेनिक बिल्कुल भी नहीं होता है। बैटरी प्रचालन के दौरान जिस ग्रिड पर रिकवरी होती है, अर्थात्। कैथोड को नष्ट नहीं किया जा सकता है। यहां तक कि अगर स्टिबाइन को किसी भी तरह से छोड़ा गया था, तो यह तुरंत PbSO4 के साथ बातचीत करेगा, इसे धातु में कम कर देगा।
हालाँकि, यहाँ एक व्यावहारिक समस्या है। गैसीय हाइड्रोजन और ऑक्सीजन मईइसके साथ इलेक्ट्रोलाइट बूंदों को खींचें, सल्फ्यूरिक एसिड का एरोसोल बनाएं। सल्फ्यूरिक एसिड का एक एरोसोल, यहां तक कि केंद्रित भी, मनुष्यों के लिए खतरनाक नहीं है और केवल खांसी का कारण बनता है। हालांकि, सल्फ्यूरिक एसिड कपड़े और कागज के लिए एक बुरा सपना है। कपड़ों पर सल्फ्यूरिक एसिड की थोड़ी मात्रा भी मिलनी चाहिए और छेद निश्चित रूप से दिखाई देंगे या इस जगह पर कपड़ा फट जाएगा। हफ्तों में, अगर बहुत तेजाब है, तो एक महीने में, लेकिन कपड़े खराब हो जाएंगे।
इसलिए आपको घरेलू दृष्टिकोण से गैस उत्सर्जन से डरना नहीं चाहिए, या आपको करना चाहिए, लेकिन आपको विशेष रूप से सल्फ्यूरिक एसिड एरोसोल पर ध्यान देने की आवश्यकता है।
तो, पानी हाइड्रोजन ऑक्सीजन में विघटित होने लगा, इलेक्ट्रोलाइट में यह कम और कम हो जाता है, आगे क्या है? यदि यह एक बैटरी है जिसमें इलेक्ट्रोलाइट को केवल एक तरल परत के रूप में डाला जाता है, तो सल्फ्यूरिक एसिड की एकाग्रता में वृद्धि के कारण स्व-निर्वहन में वृद्धि शुरू हो जाएगी। यह दिलचस्प है कि यह सेल पर वोल्टेज में मामूली वृद्धि (एसिड एकाग्रता बढ़ जाती है) के साथ होगा। यही कारण है कि कार मालिकों को लगातार अपनी बैटरी (हाइड्रोमीटर का उपयोग करके) में सल्फ्यूरिक एसिड की एकाग्रता की निगरानी करनी चाहिए और वहां पानी डालना चाहिए। पानी जोड़ने की प्रक्रिया सेवा प्रक्रिया का एक आवश्यक हिस्साकोई बैटरी। उनके प्रकारों में से एक को छोड़कर, और हम इसके बारे में अभी बात करेंगे।
यह निश्चित रूप से एक बैटरी के लिए असुविधाजनक है जिसमें धातुओं, तरल खतरों के संबंध में कास्टिक की एक परत, और इसलिए सीधे तरल से छुटकारा पाने का प्रयास बहुत पहले किया गया था, लगभग पहली छमाही में शुरू हुआ 20 वीं सदी। वैसे, ऐसा नहीं है कि सल्फ्यूरिक एसिड की एक परत सीधे इलेक्ट्रोड के चारों ओर बिखर जाती है। वास्तव में, यह सस्ते मॉडल में भी इलेक्ट्रोड और उनके आसपास के विभाजकों के बीच अच्छी तरह से वितरित किया जाता है। तो, पहला विकल्प शीसे रेशा का उपयोग करना था। यह केवल सल्फ्यूरिक एसिड के साथ लगाए गए ग्लास फाइबर के साथ इलेक्ट्रोड को घेरने के लिए पर्याप्त है और अधिकांश समस्याओं का समाधान किया जाएगा। इस प्रकार की बैटरी को एजीएम (एब्जॉर्बेंट ग्लास मैट) कहा जाता है और यूपीएस के लिए ऐसी अधिकांश बैटरी। हालांकि इस तरह की छोटी फॉर्म फैक्टर बैटरियों को अक्सर ऐसी स्थिति में रखा जाता है, जिन्हें किसी भी स्थिति में संचालित किया जा सकता है, इसे पूरी तरह से स्वीकार नहीं किया जा सकता है। एक मानक सस्ते एजीएम बैटरी के कवर को खोलने से पता चलता है कि वहां कोई विशेष कवर नहीं है, और इसलिए केवल केशिका बल इलेक्ट्रोलाइट को बहने से रोकते हैं। मुझे पूरा यकीन है कि अगर आप एजीएम बैटरी को उल्टा चलाते हैं, तो एक बार चार्ज करने के बाद उसमें से गैस के दबाव में सल्फ्यूरिक एसिड निकल जाएगा।
दूसरा आम प्रकार अधिक दिलचस्प है, यह तथाकथित है। जेल बैटरी। और वे निम्नलिखित के लिए धन्यवाद प्राप्त करते हैं। यदि घुलनशील सिलिकेटों को अम्लीकृत किया जाता है, तो सिलिकिक अम्ल निकलेगा:
ना 2 SiO 3 + H 2 SO 4 = Na 2 SO 4 + SiO2+ H2O
यदि मूल सिलिकेट घोल खराब गुणवत्ता का है, तो सिलिकिक एसिड एक कांच के द्रव्यमान के रूप में अलग हो जाएगा, लेकिन यदि यह पर्याप्त रूप से शुद्ध है, तो सिलिकिक एसिड सजातीय पारभासी जेल के एक सुंदर टुकड़े के रूप में अवक्षेपित हो जाएगा। यह प्राप्त करने की विधि का आधार है जेल बैटरी- इलेक्ट्रोलाइट में सिलिकेट्स का सरल जोड़ इसे जेल जैसे द्रव्यमान में सख्त कर देता है। तदनुसार, वहाँ से बाहर निकलने के लिए कुछ भी नहीं है और बैटरी को वास्तव में किसी भी स्थिति में संचालित किया जा सकता है। जेल बनाने की प्रक्रिया स्वयं बैटरी की क्षमता में वृद्धि नहीं करती है और इसकी गुणवत्ता में सुधार नहीं करती है, हालांकि, निर्माता इसका उपयोग उच्चतम गुणवत्ता वाले मॉडल के उत्पादन में करते हैं, और इसलिए ये बैटरी उच्च गुणवत्ता वाली होती हैं और बड़ी क्षमता. दिलचस्प बात यह है कि दोनों ही मामलों में, इलेक्ट्रोलाइट वाहक एक या दूसरे रूप में SiO2 है।
दोनों प्रकार की बैटरियों को शानदार प्रकार VRLA - वाल्व-विनियमित लेड-एसिड बैटरी में संयोजित किया जाता है, जिसका उपयोग UPS में किया जाता है। औपचारिक रूप से, उन्हें किसी भी स्थिति में अप्राप्य और स्थायी संचालन माना जाता है, लेकिन यह पूरी तरह से सच नहीं है। इसके अलावा, कई लोग पहले ही प्रभाव से मिल चुके हैं जब कुछ मिलीलीटर पानी यूपीएस से प्रतीत होने वाली मृत बैटरी को जीवन में वापस लाता है। यह इस तरह से निकलता है, क्योंकि ये बैटरियां इलेक्ट्रोलाइट में पानी के इलेक्ट्रोलिसिस से थोड़ी प्रतिरक्षा नहीं होती हैं, और, परिणामस्वरूप, सूखने से। सब कुछ ठीक वैसा ही होता है जैसा बड़े आकार की बैटरी में होता है। लेकिन सबसे महंगी और सबसे अच्छी रखरखाव-मुक्त बैटरियों में पानी में वापस छोड़ी गई गैसों के पुनर्संयोजन के लिए एक उत्प्रेरक होता है, और अब उनका मामला वास्तव में पूरी तरह से सील कर दिया गया है। मैं इस तथ्य पर आपका ध्यान आकर्षित करता हूं कि एजीएम और जीईएल प्रकार की बैटरी भी वास्तव में सील और रखरखाव मुक्त हो सकती है, लेकिन उनमें ऑक्सीजन और हाइड्रोजन पुनर्संयोजन उत्प्रेरक नहीं हो सकता है और नहीं भी हो सकता है। फिर, प्रतीत होता है कि उन्नत डिजाइन के बावजूद, उपयोगकर्ता को या तो अधिक बार नई बैटरी खरीदनी होगी, या एक सिरिंज के साथ पानी जोड़ना होगा।
मैं डिस्चार्ज मोड के बारे में कुछ शब्द जोड़ना चाहूंगा। बैटरी निर्माता किसी विशेष मॉडल के लिए अधिकतम करंट का संकेत देते हैं, लेकिन आपको यह समझने की जरूरत है कि बैटरी सिर्फ एक मिश्रण है रासायनिक पदार्थऔर ईएमएफ विशेष रूप से रासायनिक माध्यमों से उत्पन्न होता है। यह एक संधारित्र नहीं है, जिसे इलेक्ट्रो-हाइड्रोलिक सादृश्य द्वारा, एक प्रकार के यांत्रिक पोत (एक लचीली झिल्ली के साथ) के साथ तुलना की जा सकती है। हालाँकि बैटरियाँ बहुत अधिक धाराएँ प्रदान कर सकती हैं, लेकिन वास्तव में वे सबसे अच्छी तरह से संचालित होती हैं जब नहीं उच्च धाराएंडिस्चार्ज में क्या है, चार्ज में क्या है। इसलिए, छोटी बैटरी को चार्ज करने के लिए डिज़ाइन किए गए यूपीएस, जब बड़ी बैटरी के साथ काम करते हैं, तो उन्हें सबसे कोमल मोड में चार्ज किया जाएगा। हालांकि, एक दिन के भीतर नहीं। यह ध्यान रखना दिलचस्प है कि यूपीएस की शक्ति जितनी अधिक होती है, उतनी ही अधिक बैटरी निर्माता श्रृंखला में इकट्ठा करना पसंद करते हैं। यहां सब कुछ तार्किक है - छोटी बैटरी बड़ी निर्वहन धाराओं का बहुत खराब तरीके से सामना करती हैं।
उपसंहार:
1. छोटी और बड़ी बैटरी डिजाइन में समान हैं।
2. किसी भी आकार की अधिकांश बैटरियों के लिए, पानी के साथ टॉप अप करना नियमित रखरखाव का एक आवश्यक हिस्सा है।
3. केवल कुछ महंगे बैटरी मॉडल में गैस पुनर्संयोजन तंत्र होता है और इसे वास्तव में रखरखाव-मुक्त कहा जा सकता है।
4. अपने आप में, हाइड्रोजन, जो बैटरी के चार्जिंग के दौरान जारी होता है (और यह यूपीएस में निरंतर काम के बराबर है), कोई महत्वपूर्ण खतरा या समस्या नहीं है।
5. आपको बैटरी के साथ बहुत सावधानी से काम करने की ज़रूरत है, ध्यान से इलेक्ट्रोलाइट की छोटी-छोटी बूंदों को भी गिराने से बचें, या अपने कपड़े खो दें।
6. छोटी धाराओं के साथ डिस्चार्ज और चार्ज बैटरी ऑपरेशन के सबसे पसंदीदा तरीके हैं।
कुल ऊर्जा क्षमता के अनुसार, लेड-एसिड बैटरी पहले स्थान पर है। डिजाइन और इस्तेमाल किया गया एक बड़ी संख्या कीबैटरी विकल्प डिजाइन और उद्देश्य दोनों में भिन्न हैं। एसिड बैटरी की किस्में प्रसिद्ध हीलियम बैटरी हैं, साथ ही अवशोषित इलेक्ट्रोलाइट वाली बैटरी, एजीएम तकनीक का उपयोग करके बनाई गई हैं। हालांकि, उन सभी में कई सामान्य विशेषताएं हैं जो एसिड बैटरी के लिए अद्वितीय हैं। इसलिए, एसिड बैटरी के संचालन की प्रक्रियाओं और विशेषताओं की बेहतर समझ के लिए, खुली और बंद प्रकार की तरल इलेक्ट्रोलाइट वाली पहली पीढ़ी की बैटरी से अधिक परिचित होना आवश्यक है।
ऐसी बैटरियों के साथ, ऑपरेटिंग मोड को नियंत्रित करना और विनियमित करना आसान होता है और जब सही संचालनवे काफी लंबे समय तक चलते हैं। अब शायद ही कभी स्थिर खुली बैटरियों का उपयोग किया जाता है, जिनमें आधुनिक मानकों द्वारा भी बहुत अच्छी विशेषताएं हैं। यह रखरखाव की कठिनाइयों के कारण है, उन्हें एक विशेष कमरे, वेंटिलेशन की आवश्यकता होती है। एक नियम के रूप में, एक पारदर्शी, दृश्यमान कांच का मामला, प्लेटों और इलेक्ट्रोलाइट तक आसान पहुंच, उचित संचालन के साथ, ऐसी बैटरी को दशकों तक उपयोग करने की अनुमति देता है।
बंद बैटरी, आमतौर पर भरने और इलेक्ट्रोलाइट नियंत्रण के लिए प्लग के साथ गैर-वियोज्य, कई किस्में होती हैं और उन्हें उनके उद्देश्य, चार्जिंग विधि, डिज़ाइन सुविधाओं और सामग्री के अनुसार वर्गीकृत किया जाता है। इस तरह की बैटरियों का व्यापक रूप से उपयोग किया जाता है, मुख्य रूप से मोटर वाहन और ट्रैक्टर प्रौद्योगिकी में स्टार्टर बैटरी के रूप में, कुछ प्रकार के विद्युत परिवहन के लिए ट्रैक्शन बैटरी के रूप में, और बैकअप और आपातकालीन शक्ति के स्थिर स्रोतों के रूप में। उनकी विशेषताओं के अनुसार, उन्हें ऑपरेशन के बफर मोड में या चक्रीय मोड में संचालन के लिए इच्छित में विभाजित किया गया है। हाल ही में, तरल इलेक्ट्रोलाइट वाली बैटरियों को तेजी से रखरखाव-मुक्त बैटरियों द्वारा प्रतिस्थापित किया जा रहा है, जिन्होंने बड़े पैमाने पर सेवित लोगों के फायदे और नुकसान को अपनाया है।
एसिड बैटरी के मुख्य लाभ कम लागत, लंबी सेवा जीवन, उच्च डिस्चार्ज करंट, कम सेल्फ-डिस्चार्ज करंट हैं। सामान्य नुकसान में प्रति किलोग्राम वजन में कम ऊर्जा खपत, लंबे समय तक चार्ज करने का समय, तापमान पर विशेषताओं की उच्च निर्भरता, और एक निर्वहन राज्य में दीर्घकालिक भंडारण की अनुमति नहीं है।
प्रत्येक बैटरी में एक इलेक्ट्रोलाइट समाधान में डूबे हुए विपरीत इलेक्ट्रोड होते हैं और एक टिकाऊ, रासायनिक रूप से प्रतिरोधी मामले में रखे जाते हैं।
विभिन्न बैटरी इलेक्ट्रोड को एक या अधिक तत्वों में संयोजित किया जाता है, जिन्हें अन्यथा बैटरी बैंक कहा जाता है। एक आवेशित कैन का वोल्टेज 2.1 V है, और एक डिस्चार्ज कैन 1.8 V है। प्रत्येक में दो इलेक्ट्रोड या एक ही नाम के इलेक्ट्रोड के दो समूह हो सकते हैं, जो अधिक क्षमता के लिए समानांतर में जुड़े होते हैं। चूँकि धनात्मक प्लेटों को ऋणात्मक प्लेटों के बीच स्थित होना चाहिए, इसलिए ऋणात्मक प्लेटों की संख्या हमेशा धनात्मक प्लेटों की संख्या से एक अधिक होती है। इस स्थिति के तहत, सकारात्मक प्लेटों के दोनों पक्ष इलेक्ट्रोलाइट के साथ परस्पर क्रिया करते हैं (एक तरफा संचालन के दौरान, सकारात्मक प्लेट ताना और नकारात्मक प्लेटों के संपर्क में शॉर्ट सर्किट हो सकता है)।
एक मामले में, कई बैटरी सेल आमतौर पर रखी जाती हैं, जो एक बैटरी से जुड़ी होती हैं। बैटरी वोल्टेज कोशिकाओं की संख्या पर निर्भर करता है। सबसे अधिक बार, तथाकथित बारह-वोल्ट बैटरी छह कोशिकाओं से बनी होती हैं। कम सामान्यतः, छह-वोल्ट या चौबीस वोल्ट की बैटरी का उत्पादन किया जाता है। वास्तविक वोल्टेजबैटरी के आवेश की स्थिति और इलेक्ट्रोलाइट के घनत्व पर निर्भर करता है।
15 0 C के तापमान पर इलेक्ट्रोलाइट का अनुशंसित घनत्व 1.29 है, पूरी तरह से चार्ज और सामान्य तापमान. ऊंचे तापमान पर चलने वाली एसिड बैटरियों के लिए, इलेक्ट्रोलाइट का घनत्व लगभग 1.25 तक कम हो जाता है। कम तापमान पर, तापमान के आधार पर इलेक्ट्रोलाइट के घनत्व को लगभग 1.3 या अधिक तक बढ़ाने की सिफारिश की जाती है। इलेक्ट्रोलाइट का घनत्व उसके तापमान के साथ अलग-अलग होगा, इसलिए घनत्व का निर्धारण करते समय तापमान सुधार को ध्यान में रखा जाना चाहिए।
| 0С . मापते समय तत्व का तापमान | समाधान तापमान में लाने के लिए संशोधन, जी/सेमी 3 | ||
|---|---|---|---|
| 15 0 सी | 20 0 सी | 30 0 सी | |
| +60 | 0,031 | 0,024 | 0,021 |
| +45 | 0,021 | 0,014 | 0,01 |
| +30 | 0,01 | 0,004 | 0 |
| +25 | 0,007 | 0 | -0,004 |
| +15 | 0 | -0,007 | -0,001 |
| 0 | -0,01 | -0,017 | -0,021 |
| -15 | -0,021 | -0,028 | -0,031 |
| -25 | -0,28 | -0,035 | -0,038 |
| -30 | 0,01 | 0,004 | 0 |
| -45 | -0,04 | -0,049 | -0,052 |
| -50 | -0,046 | -0,053 | -0,055 |
घनत्व, आदर्श से 0.01 ग्राम / सेमी 3 कम हो गया, 6% की श्रेणी से मेल खाता है। पूरी तरह से डिस्चार्ज की गई बैटरी में इलेक्ट्रोलाइट घनत्व 1.10 ± 0.01 g/cm 3 है। हालांकि, यह याद रखना चाहिए कि तापमान के लिए एसिड मीटर की रीडिंग को सही किया जाना चाहिए। इलेक्ट्रोलाइट का घनत्व +25 0 सी के तापमान पर 1.27-1.28 ग्राम / सेमी 3 के बराबर होना चाहिए। +5-10 0 सी के तापमान पर, यह तापमान पर लगभग 0.01 ग्राम / सेमी 3 बढ़ जाता है - 10 डिग्री सेल्सियस - 0.02 ग्राम / सेमी 3 पर - 25 डिग्री सेल्सियस - 0.03 ग्राम / सेमी 3 से। इलेक्ट्रोलाइट का घनत्व तब नहीं मापा जाता जब इलेक्ट्रोलाइट का स्तर असामान्य हो, जब इलेक्ट्रोलाइट "उबल रहा हो" या बहुत गर्म हो। बैटरी की बैटरी में इलेक्ट्रोलाइट का घनत्व 0.01 ग्राम / सेमी 3 से अधिक नहीं होना चाहिए। अन्यथा, बैटरी को चार्ज किया जाना चाहिए और बैटरी में पानी या इलेक्ट्रोलाइट जोड़कर इलेक्ट्रोलाइट के घनत्व को ठीक किया जाना चाहिए। यदि घनत्व आदर्श से ऊपर है, तो पानी जोड़ा जाता है, यदि यह कम है, तो 1.4 ग्राम / सेमी 3 के घनत्व वाला इलेक्ट्रोलाइट जोड़ा जाता है। बैटरी से प्रारंभिक चयन के बाद टॉपिंग किया जाता है सही मात्राइलेक्ट्रोलाइट. फिर बैटरीइलेक्ट्रोलाइट को पूरी तरह से मिलाने के लिए 25 - 30 मिनट के लिए चार्ज करें और फिर से इसके घनत्व को मापें।
यह ध्यान में रखा जाना चाहिए कि सर्दियों में, इलेक्ट्रोलाइट के कम प्रारंभिक घनत्व और बैटरी के एक बड़े निर्वहन के साथ, इलेक्ट्रोलाइट जम सकता है। उदाहरण के लिए, पूरी तरह से डिस्चार्ज की गई बैटरी में 1.30 ग्राम / सेमी 3 के प्रारंभिक घनत्व के साथ, इलेक्ट्रोलाइट -14 डिग्री सेल्सियस पर जम सकता है, लेकिन यदि इलेक्ट्रोलाइट का प्रारंभिक घनत्व 1.24 ग्राम / सेमी 3 है, तो एक डिस्चार्ज की गई बैटरी जम जाएगी पहले से ही -5 डिग्री सेल्सियस पर।
एक लेड बैटरी के सक्रिय पदार्थ जो रासायनिक धारा-उत्पादक प्रतिक्रियाओं में भाग लेते हैं, वे हैं:
सकारात्मक इलेक्ट्रोड पर - लेड डाइऑक्साइड PbO2 (गहरा भूरा);
नकारात्मक इलेक्ट्रोड पर - स्पंजी लेड Pb (ग्रे);
इलेक्ट्रोलाइट - सल्फ्यूरिक एसिड का जलीय घोल H2SO4
जब बैटरी को डिस्चार्ज किया जाता है, तो नकारात्मक इलेक्ट्रोड का सक्रिय द्रव्यमान
स्पंजी लेड से लेड सल्फेट में बदल जाता है, और रंग ग्रे से हल्के भूरे रंग में बदल जाता है, दो इलेक्ट्रॉनों को विद्युत सर्किट में दान करता है।
Pb + H2SO4 → PbSO4 + H+ + 2e-
निर्वहन के दौरान सकारात्मक इलेक्ट्रोड का सक्रिय द्रव्यमान डाइऑक्साइड से परिवर्तित हो जाता है
लीड PbO2, साथ ही नकारात्मक इलेक्ट्रोड के सक्रिय द्रव्यमान, लेड सल्फेट में
PbSO4 गहरे भूरे से हल्के भूरे रंग में बदल जाता है, दो को अवशोषित करता है
इलेक्ट्रॉन।
PbO2 + H2SO4 + 3H+ + 2e- → PbSO4 + 2H2O
बैटरी डिस्चार्ज के परिणामस्वरूप, सकारात्मक (PbO2) और . दोनों की सक्रिय सामग्री
नकारात्मक (Pb) इलेक्ट्रोड लेड सल्फेट PbSO4 में परिवर्तित हो जाते हैं। साथ ही, पर
लेड सल्फेट के निर्माण में सल्फ्यूरिक एसिड की खपत होती है, जिससे कमी होती है
इलेक्ट्रोलाइट एकाग्रता और, परिणामस्वरूप, इसके घनत्व में कमी। कुल
बैटरी डिस्चार्ज होने पर प्रतिक्रिया:
PbO2 + Pb + 2H2SO4 → 2PbSO4 + 2H2O
जब बैटरी को चार्ज किया जाता है, तो रिवर्स रासायनिक प्रक्रियाएं होती हैं विपरीत दिशा, जिसके दौरान, अन्य बातों के अलावा, सल्फ्यूरिक एसिड का निर्माण होता है, जिसके परिणामस्वरूप चार्जिंग के दौरान इलेक्ट्रोलाइट का घनत्व बढ़ जाता है। चार्ज प्रक्रिया का कुल समीकरण:
2PbSO4 + 2H2O → PbO2 + Pb + 2H2SO4
जब सकारात्मक के सक्रिय द्रव्यमान में पदार्थों के परिवर्तन की प्रतिक्रियाएं और
नकारात्मक इलेक्ट्रोड पूरे हो जाते हैं, इलेक्ट्रोलाइट का घनत्व बदलना बंद हो जाता है,
जो बैटरी चार्ज के अंत को इंगित करता है। आगे के साथ
चार्ज की निरंतरता तथाकथित माध्यमिक प्रक्रिया को आगे बढ़ाती है -
पानी का ऑक्सीजन और हाइड्रोजन में इलेक्ट्रोलाइटिक अपघटन। से अलग
इलेक्ट्रोलाइट गैस के बुलबुले के रूप में, वे इलेक्ट्रोलाइट उबलने का भ्रम पैदा करते हैं, जो
चार्जिंग प्रक्रिया के पूरा होने के संकेत के रूप में भी कार्य करता है।
सभी बैटरियां डिस्चार्ज होने पर जितनी ऊर्जा दे सकती हैं, उससे अधिक ऊर्जा की खपत करती हैं। अधिकांश ऊर्जा हीटिंग में जाती है, और कुछ हिस्सा इलेक्ट्रोलाइट के इलेक्ट्रोलिसिस पर खर्च किया जाता है। डिस्चार्ज के दौरान बैटरी से प्राप्त ऊर्जा का उसके चार्ज पर खर्च की गई ऊर्जा के अनुपात को बैटरी का ऊर्जा उत्पादन कहा जाता है और एसिड बैटरी के लिए यह अनुपात औसतन 0.65 होता है।
बेहतर इलेक्ट्रोलाइट परिसंचरण और रासायनिक प्रतिक्रिया के लिए बैटरी इलेक्ट्रोड में छिद्रपूर्ण संरचना होती है। सबसे अधिक बार, इलेक्ट्रोड सक्रिय पदार्थ से भरी कोशिकाओं के साथ एक लीड ग्रिड से बने होते हैं। इलेक्ट्रोड को छेद या जाल के साथ विद्युत इन्सुलेट सामग्री से बने विभाजक द्वारा अलग किया जाता है। इलेक्ट्रोड के निचले किनारों को उठाया जाता है ताकि ढीला कीचड़ इलेक्ट्रोड को छोटा न करे। इलेक्ट्रोड की फिलिंग को बेहतर बनाए रखने और उखड़ने नहीं देने के लिए, शीसे रेशा या छिद्रों के साथ हार्ड लाइनिंग से बने अतिरिक्त सुरक्षा का उपयोग किया जाता है। ऐसे इलेक्ट्रोड को बख्तरबंद कहा जाता है।
हाल ही में, इलेक्ट्रोड में एडिटिव्स, इलेक्ट्रोड फिलिंग, साथ ही इलेक्ट्रोलाइट में एडिटिव्स का तेजी से उपयोग किया गया है।
शुद्ध लेड से बने ग्रिड के इलेक्ट्रोड में कम कठोरता होती है और उच्च धाराओं के साथ-साथ यांत्रिक प्रभावों के साथ, वे ताना कर सकते हैं, ग्रिड का भरना फैल जाता है। यांत्रिक शक्ति को बढ़ाने के लिए, लेड में सुरमा मिलाया जाता है। यह, बदले में, ऑपरेशन के दौरान हाइड्रोजन और ऑक्सीजन की रिहाई को बढ़ाने के लिए बैटरी इलेक्ट्रोलाइट की प्रवृत्ति को कुछ हद तक बढ़ा देता है। 1970 के दशक की शुरुआत में, दोनों इलेक्ट्रोडों में कैल्शियम मिलाया गया था। गैसों का उत्सर्जन काफी कम हो गया था और निर्माताओं ने रखरखाव मुक्त बैटरी की उपस्थिति के बारे में बात करना शुरू कर दिया था। लेड-कैल्शियम बैटरियां डीप चार्ज और डिस्चार्ज साइकल को खराब सहन करती हैं। 6 डिब्बे के लिए ऐसी बैटरियों के लिए, एक पूर्ण चार्ज के लिए, आपको वोल्टेज को 14.8V तक बढ़ाने की आवश्यकता है। एक समझौता विकल्प हाइब्रिड बैटरी थी। ऐसी बैटरियों में, सकारात्मक जाली सुरमा के साथ मिश्र धातु से बनी होती है, और नकारात्मक जाली कैल्शियम से बनी होती है। पानी की खपत बहुत कम हो गई है, हालांकि अभी भी नियमित स्तर की जांच की सिफारिश की जाती है। हाइब्रिड बैटरी लेड-कैल्शियम की तुलना में साइकिल चलाने के लिए अधिक प्रतिरोधी हैं, लेकिन फिर भी मूल लेड-एंटीमोनी जितनी अच्छी नहीं हैं। हाइब्रिड बैटरी से लैस अधिकांश वाहनों में रेगुलेटर रिले वोल्टेज 14.3 V पर सेट होता है। इलेक्ट्रोड में कोबाल्ट, निकल, कॉपर भी शामिल हो सकते हैं।
कुछ एडिटिव्स का उपयोग इलेक्ट्रोड की स्थिरता को बढ़ाने के लिए किया जाता है, जैसे कालिख। मुख्य रूप से गहरे निर्वहन के दौरान प्लेट सल्फाइटेशन को कम करने के लिए रखरखाव से मुक्त बैटरीइलेक्ट्रोलाइट में लगाए गए एडिटिव्स का उपयोग किया जाता है, उदाहरण के लिए, बेरियम सल्फेट, स्ट्रोंटियम सल्फेट, फॉस्फोरिक एसिड। स्व-निर्वहन को कम करने के लिए, दर्ज करें कार्बनिक पदार्थ- अवरोधक, उदाहरण के लिए, अल्फ़ानाफ्थोल। बैटरी के कुछ गुणों में सुधार करके, एडिटिव्स अन्य विशेषताओं को खराब कर सकते हैं, इसलिए एडिटिव्स के सेट को आवश्यक गुणों के आधार पर प्रत्येक प्रकार की बैटरी के लिए व्यक्तिगत रूप से चुना जाता है।
एसिड बैटरीओवरचार्जिंग की अनुमति दे सकता है, लेकिन फिर अतिरिक्त ऊर्जा का उपयोग बैटरी को गर्म करने और पानी को इलेक्ट्रोलाइज करने के लिए किया जाता है। इसलिए, यदि इलेक्ट्रोलाइट का स्तर तेजी से गिरता है, तो आपको आसुत जल जोड़ने और चार्ज रेगुलेटर पर वोल्टेज कम करने की आवश्यकता है। इलेक्ट्रोलाइट के उबलने को कम करने के लिए, एक विशेष डिजाइन के वाल्व के साथ प्लग बनाए जाते हैं जो इलेक्ट्रोलाइट एरोसोल की रिहाई को बाधित करते हैं। वाल्व के साथ प्लग का मुख्य उद्देश्य बैटरी के विनाश को रोकने के साथ-साथ वायुमंडलीय हवा से सुरक्षा करना है। सेवित बैटरियों के लिए, प्लग का उपयोग इलेक्ट्रोलाइट या आसुत जल भरने के लिए भी किया जाता है। उत्प्रेरक के साथ प्लग का उपयोग पुनर्प्राप्ति को बढ़ावा देने के लिए भी किया जाता है ( रासायनिक यौगिक) हाइड्रोजन और ऑक्सीजन परमाणु वापस पानी में।
लेड-एसिड बैटरियों को जल्दी चार्ज नहीं किया जा सकता। अनुशंसित चार्ज मोड के अनुसार, लीड-एसिड बैटरी को बफर मोड में चार्ज करने के लिए डिज़ाइन किया गया है और चक्रीय मोड में चार्ज करने के लिए डिज़ाइन किया गया है। बफर मोड में, बैटरी लगभग हमेशा चार्ज मोड में होती हैं, दूसरे वोल्टेज स्रोत से सक्रिय होती हैं और साथ ही लोड से जुड़ी होती हैं। निर्वहन अपेक्षाकृत कम ही होता है, उपभोक्ता के चरम भार पर, जब मुख्य ऊर्जा स्रोत आवश्यक शक्ति प्रदान नहीं कर सकता है। इसके अलावा, बैटरी को एक आपातकालीन स्रोत के रूप में काम करना चाहिए और ऊर्जा के मुख्य स्रोत के संचालन में छोटी रुकावटों के दौरान ऊर्जा देना चाहिए। इस मोड में, मुख्य ऊर्जा स्रोत से वोल्टेज पूरी तरह चार्ज बैटरी के वोल्टेज से काफी अधिक होता है। यदि बैटरी को डिस्चार्ज किया जाता है, उदाहरण के लिए, मुख्य ऊर्जा स्रोत के आपातकालीन शटडाउन के दौरान, तो चार्जिंग के प्रारंभिक चरण में, चार्ज करंट काफी बड़ा होगा और कुछ ही घंटों में बैटरी अपनी क्षमता के आधे से अधिक हासिल कर लेगी। तब रिचार्ज की गई बैटरी और मुख्य शक्ति स्रोत के वोल्टेज के बीच का अंतर छोटा हो जाएगा और अंतिम चार्ज एक छोटे से करंट के साथ लंबे समय तक चलता रहेगा। एक सटीक वोल्टेज सेटिंग के साथ, चार्ज करने के बाद बैटरी बहुत कम करंट की खपत करेगी, जो बैटरी के स्व-निर्वहन के लिए क्षतिपूर्ति करती है, और इस मोड में यह बहुत बनी रह सकती है बड़ा समय. इस मोड में, आपातकालीन और बैकअप बैटरी संचार प्रणालियों, स्वचालन, सुरक्षा उपकरणों, निर्बाध बिजली आपूर्ति के लिए काम करती हैं।
चक्रीय चार्ज मोड में, बैटरी को चार्ज करने के लिए आवश्यक एक निश्चित समय के लिए चार्ज पर रखा जाता है, और फिर इसे चार्जर से डिस्कनेक्ट कर दिया जाता है और डिस्चार्ज मोड में काम करने के लिए रख दिया जाता है। इस मोड में, पोर्टेबल डिवाइस के साथ-साथ इलेक्ट्रिक वाहन भी काम करते हैं। इस मोड में चार्जिंग आमतौर पर 8-16 घंटों के भीतर हो जाती है। अनुशंसित चार्जिंग करंट आमतौर पर 0.1C (बैटरी क्षमता का दसवां हिस्सा) होता है। हालांकि, चार्जिंग के शुरुआती चरण में, कुछ ब्रांड की बैटरियों के लिए 0.3C तक के चार्जिंग करंट की अनुमति है। चार्ज के अंत में, जब प्रचुर मात्रा में गैसिंग शुरू होती है, तो वर्तमान को 0.05C तक कम करने की सिफारिश की जाती है। आमतौर पर, वर्तमान सीमा के साथ, वांछित वोल्टेज सेट करके चार्ज मोड किया जाता है। अलग-अलग चार्जर में अलग-अलग मोड और क्षमताएं होती हैं। चार्ज वोल्टेज और चार्ज करंट आपस में जुड़े हुए हैं। इसलिए, एक निश्चित प्रकार की बैटरी क्षमता के लिए चार्जर चुनना आवश्यक है। एक पूर्ण और सुरक्षित चार्ज के लिए, बैटरी को कई चक्रों में चार्ज करने की अनुशंसा की जाती है। प्रत्येक चक्र का अपना वोल्टेज और चार्ज करंट होना चाहिए। इसके अलावा, यह अनुशंसा की जाती है कि सल्फाइटेशन को हटाने और रोकने के लिए कम से कम एक या दो चक्र स्पंदित, कभी-कभी विषम धारा के साथ किए जाएं। ऐसे कई चक्रों को स्वचालित रूप से स्विच करने के लिए प्रोग्राम किए गए चार्जर बहुत दुर्लभ हैं, और विभिन्न लेखकों द्वारा अनुशंसित चार्ज मोड भिन्न होते हैं। यह सिर्फ इतना है कि पल्स चार्जर काफी किफायती हैं, लेकिन इन उपकरणों की चार्जिंग सुविधाओं का अभी तक पर्याप्त अध्ययन और काम नहीं किया गया है।
लीड-एसिड बैटरी के संचालन की मुख्य विशेषताएं। बड़े डिस्चार्ज करंट के साथ, कैपेसिटेंस छोटा होता है, तापमान में कमी के साथ कैपेसिटेंस गिर जाता है। ऊंचे तापमान, उच्च चार्ज और डिस्चार्ज धाराओं, कम इलेक्ट्रोलाइट स्तर और अनुचित घनत्व के साथ-साथ एक डिस्चार्ज अवस्था में गहरे निर्वहन और भंडारण पर सेवा जीवन कम हो जाता है। इन शर्तों के तहत, एसिड बैटरी का सेवा जीवन अधिकतम होगा।
